A-J是中学化学中常见的物质。其中A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。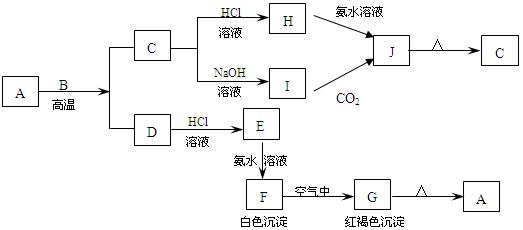
(1)写出下列物质的化学式:
A , J 。
(2)按要求书写有关方程式:
D与稀HCl反应的离子方程式 ;
B与NaOH溶液反应的化学方程式 。
A-J是中学化学中常见的物质。其中A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。
(1)写出下列物质的化学式:
A , J 。
(2)按要求书写有关方程式:
D与稀HCl反应的离子方程式 ;
B与NaOH溶液反应的化学方程式 。