(12分))某有机化合物A经李比希法测得其中含碳为72.0%、含氢为6.67%,其余为氧。现用下列方法测定该有机化合物的相对分子质量和分子结构。
方法一:用质谱法分析得知A的相对分子质量为150。
方法二:核磁共振仪测出A的核磁共振氢谱有5个峰,其面积之比为1∶2∶2∶2∶3,如图A所示。
方法三:利用红外光谱仪测得A分子的红外光谱如图B所示。

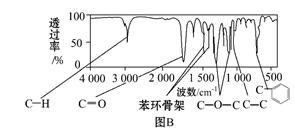
请填空:
(1)A的分子式为 。
(2)A的分子中含一个甲基的依据是 。
a.A的相对分子质量
b.A的分子式
c.A的核磁共振氢谱图
d.A分子的红外光谱图
(3)A的结构简式为 。