孔雀石主要含Cu2(OH)2CO3〔也可认为是Cu(OH)2·CuCO3〕,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O,步骤如下: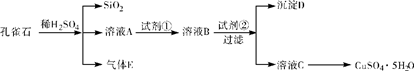
 请回答下列问题:(1)气体E的化学式是 。
请回答下列问题:(1)气体E的化学式是 。
(2)由溶液C获得CuSO4·5H2O,需要经过蒸发浓缩、冷却结晶、 和干燥等操作。
(3)写出孔雀石主要成分与稀硫酸反应的化学方程式: 。
孔雀石主要含Cu2(OH)2CO3〔也可认为是Cu(OH)2·CuCO3〕,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O,步骤如下:
 请回答下列问题:(1)气体E的化学式是 。
请回答下列问题:(1)气体E的化学式是 。
(2)由溶液C获得CuSO4·5H2O,需要经过蒸发浓缩、冷却结晶、 和干燥等操作。
(3)写出孔雀石主要成分与稀硫酸反应的化学方程式: 。