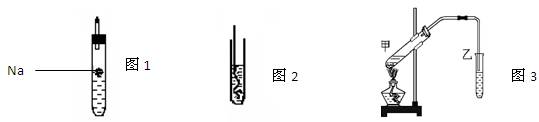
(14分)某同学设计如图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:

实验
|
药品
|
制取气体
|
量气管中的液体
|
Ⅰ
|
Cu、稀HNO3
|
|
H2O
|
Ⅱ
|
NaOH固体、浓氨水
|
NH3
|
|
Ⅲ
|
Na2SO3固体、浓H2SO4[来
|
SO2
|
|
Ⅳ
|
镁铝合金、NaOH溶液(足量)
|
H2
|
H2O
|
⑴实验过程中,使用分液漏斗滴加液体的操作是。
⑵该同学认为实验I可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?(填“可行”或“不可行”),原因是.
⑶实验Ⅲ烧瓶中产生的SO2气体通入溴水溶液中,现象是.发生反应的离子方程式 是.
是.
⑷实验Ⅱ中量气管中的液体最好是____(填字母编号,下同)
a.浓NaOH溶液 b.氨水 c.煤油 d.氯化铵溶液
该实验剩余的NH3需吸收处理.以下各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有.

⑸本实验应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,②,③视线与凹液面最低处相平.
⑹实验Ⅳ获得以下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
编号
|
镁铝合金度量
|
量气管第一次读数
|
量气管第二次读数
|
①
|
1.0g
|
10.0mL
|
346.3mL
|
②
|
1.0g
|
10.0mL
|
335.0mL
|
③
|
1.0g
|
10.0mL
|
345.7mL
|
根据上述数据,可计算出镁铝合金中铝的质量分数为____.

 实验现象
实验现象 溶液等。
溶液等。

 质量
质量
 是.
是.
 粤公网安备 44130202000953号
粤公网安备 44130202000953号