A是生产某新型工程塑料的基础原料之一,结构简式为: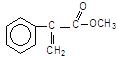
(1)写出A分子式的_____ ______
(2)拟从芳香烃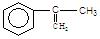 出发来合成A,其合成路线如下:
出发来合成A,其合成路线如下:
已知:A在酸性条件下水解生成有机物B和甲醇。
(a)写出⑤反应类型__________ (b)写出H的结构简式__________
(c)已知F分子中含有“—CH2OH”,通过F不能有效、顺利地获得B,其原因是 ________
(d)两分子H之间发生反应生成六元环酯结构简式是: 。
A是生产某新型工程塑料的基础原料之一,结构简式为:
(1)写出A分子式的_____ ______
(2)拟从芳香烃 出发来合成A,其合成路线如下:
出发来合成A,其合成路线如下:
已知:A在酸性条件下水解生成有机物B和甲醇。
(a)写出⑤反应类型__________ (b)写出H的结构简式__________
(c)已知F分子中含有“—CH2OH”,通过F不能有效、顺利地获得B,其原因是 ________
(d)两分子H之间发生反应生成六元环酯结构简式是: 。