传统制取甲醇的原理是CO(g)+ 2H2(g) CH3OH(g) ---------①
CH3OH(g) ---------①
25℃时,K=2.68×1022
最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。“绿色自由”构想技术流程如下: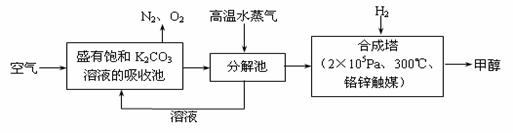
 反应原理为①CO2(g)+3H2(g) CH3OH(g)+H2O(g)------------------②
反应原理为①CO2(g)+3H2(g) CH3OH(g)+H2O(g)------------------②
25℃时,K=3.96×1011
回答:
(1)相同条件下,反应①与反应②相比,转化率更大的是 ,(用①②回答)
(2)写出反应②的平衡常数表达式K= ,
(3)在30MPa压强下,测得反应②的实验数据如下表。分析表中数据回答下列问题:
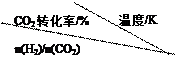 |
500 |
600 |
700 |
800 |
| 1.5 |
45 |
33 |
20 |
12 |
| 2.0 |
60 |
43 |
28 |
15 |
| 3.0 |
83 |
62 |
37 |
22 |
温度升高,K值 (填“增大”、“减小”、或“不变”)。反应的△H 0(填>、=、<)
(4)下列措施中能使n(CH3OH)/n(CO2)增大的是___________。(设合成塔为密闭容器)
| A.升高温度 | B.充入He(g) |
| C.将H2O(g)从体系中分离 | D.再充入1mol CO2和3mol H2 |
(5)甲醇可制作燃料电池。写出以氢氧化钾为电解质的甲醇燃料电池负极反应式 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号