(9分)下图中A~J均代表无机物或其水溶液,其中B、D、G是单质,A是红棕色粉末,G是气体,J是黑色晶体。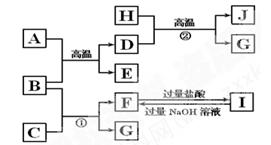
根据图示回答问题:
(1)写出下列物质的化学式:A ,E ,I ;
(2)反应②的化学方程式是 ;
(3)J与盐酸反应的化学方程式是 ;
产生等物质的量G分别消耗单质D与B 的物质的量之比
(9分)下图中A~J均代表无机物或其水溶液,其中B、D、G是单质,A是红棕色粉末,G是气体,J是黑色晶体。
根据图示回答问题:
(1)写出下列物质的化学式:A ,E ,I ;
(2)反应②的化学方程式是 ;
(3)J与盐酸反应的化学方程式是 ;
产生等物质的量G分别消耗单质D与B 的物质的量之比