(I)某氮肥厂氨氮废水中的氮元素多以NH 4 +和NH 3·H 2O的形式存在。在微生物作用下,NH 4 +经过两步反应被氧化成NO 3 -,两步反应的能量变化示意图如下:
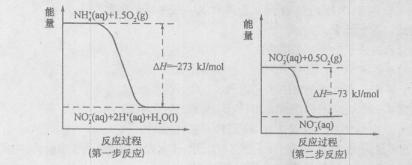
(1)1molNH 4 +(aq)全部氧化成NO 3 -(aq)的热化学方程式是  。
。
(2)在一定条件下,向废水中加入CH 3OH,将HNO 3还原成N 2,若该反应消耗32gCH 3OH转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是 。
(Ⅱ)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO 2和N 2,化学方程式如下:
2NO+2CO 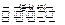 2CO 2+N 2 △H
2CO 2+N 2 △H
某温度下用气体传感器测得不同的时间的NO和CO浓度如下表:
| 时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
| C(NO)(×10 -4mol·L -1) |
10.0 |
4.50 |
2.50 |
1.50 |
1.00 |
1.00 |
| C(CO)(×10 -3mol·L -1) |
3.60 |
3.05 |
2.85 |
2.75 |
2.70 |
2.70 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H 0(填写">"、"<"、"=")
(2)前2s内的平均反应速率v(N 2)= ;
(3)在该温度下,反应的平衡常数K= (只写出计算结果);
(4)某同学设计了三组实验,分别验证温度、催化剂比表面积对化学反应速率的影响规律,部分实验条件如下表:
| 实验编号 |
T/℃ |
NO初始浓度/mol·L -1 |
CO初始浓度/mol·L -1 |
催化剂的比表面积/m 2·g -1 |
| I |
28  0 0 |
1.20×10 -3 |
5.80×10 -3 |
82 |
| II |
280 |
1.20×10 -3 |
5.80×10 -3 |
124 |
| III |
350 |
1.20×10 -3 |
5.80×10 -3 |
124 |
该同学画出了表中三个实验条件下,混合气体中NO浓度随时间变化的趋势曲线图,请在图上标明各条曲线的实验编号;
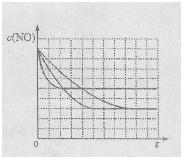
(5)有人认为:催化剂比表面积增大,会提高NO和CO的反应效率,从而使污染物NO和CO的转化率提高。请用化学基本理论对此观点进行评价: 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号