已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F。其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满。请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)
(1)A、B、C、D的第一电离能由小到大的顺序为 。(用元素符号表示)
(2)B的氯化物的熔点比D的氯化物的熔点 (填高或低),
理由是 。
(3)A的最高价氧化物对应的水化物分子中其中心原子采取 杂化,E的最高价氧化物分子的空间构型是 。
(4)F的核外电子排布式是 ,F的高价离子与A的简单氢化物形成的配离子的化学式为 .
(5)A、F形成某种化合物的晶胞结构如图所示(其中A显-3价),则其化学式为 ;(每个球均表示1个原子)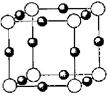
(6)A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,则其化学式为 ,其晶体中所含的化学键类型为 。
 O2(g)=CO(g)+2H2(g)△H2=-35.4 kJ·mol-1
O2(g)=CO(g)+2H2(g)△H2=-35.4 kJ·mol-1 [Cu(NH3)3]Ac·CO△H<0
[Cu(NH3)3]Ac·CO△H<0
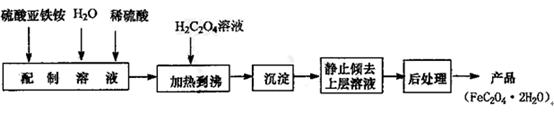
 6H2O溶液时,需加少量稀硫酸,目的是。
6H2O溶液时,需加少量稀硫酸,目的是。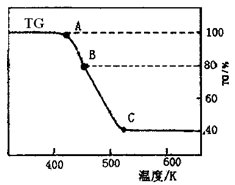
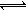 Fe(s)+CO2(g)反应平衡常数K=0.4,则该反应达平衡时,FeO的转化率为多少?。
Fe(s)+CO2(g)反应平衡常数K=0.4,则该反应达平衡时,FeO的转化率为多少?。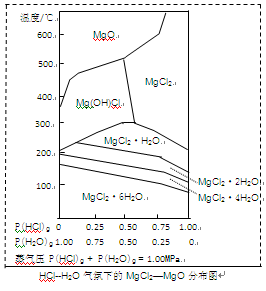
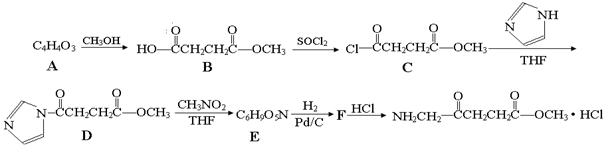
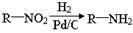
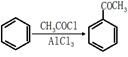 ,请结合题中所给信息,写出由CH3CH2COOH、
,请结合题中所给信息,写出由CH3CH2COOH、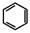 为原料合成
为原料合成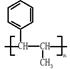 单体的合成路线流程图(无机试剂任选)。
单体的合成路线流程图(无机试剂任选)。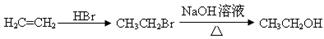
 ,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.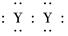 ]2-
]2-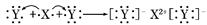
 粤公网安备 44130202000953号
粤公网安备 44130202000953号