已知有以下物质相互转化,其中A为单质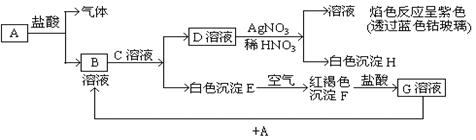
试回答:
(1)写出下列物质的化学式:
A  ;B ; H ;F
;B ; H ;F
(2)写出由A转变成B的离子反应方程式 
(3)写出用KSCN溶液鉴别G溶液的离子方程式
(4)写出G溶液加入A的有关离子反应方程式
已知有以下物质相互转化,其中A为单质
试回答:
(1)写出下列物质的化学式:
A  ;B ; H ;F
;B ; H ;F
(2)写出由A转变成B的离子反应方程式 
(3)写出用KSCN溶液鉴别G溶液的离子方程式
(4)写出G溶液加入A的有关离子反应方程式