写出下列有机物的结构简式:
(1)2,6-二甲基-4-乙基辛烷: ;
(2)2-甲基-1-戊烯: ;
(3)有A、B、C三种烃,它们的结构简式如下图所示: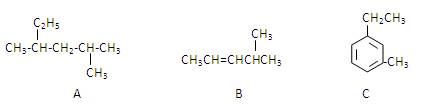
A的名称是 ;B的名称是 ;
C的名称是 。
写出下列有机物的结构简式:
(1)2,6-二甲基-4-乙基辛烷: ;
(2)2-甲基-1-戊烯: ;
(3)有A、B、C三种烃,它们的结构简式如下图所示: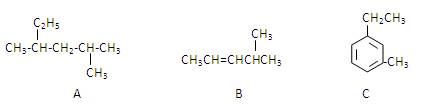
A的名称是 ;B的名称是 ;
C的名称是 。