有机物A的结构简式为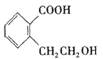 ,它可通过不同的反应生成下列物质:
,它可通过不同的反应生成下列物质: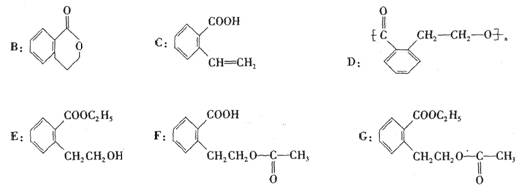
(1)在A—G中,不属于酯类的化合物有 (填写编号)。
(2)写出苯环上只有一个取代基,且组成上比A少一个碳原子的A的同系物的结构简式 。
(3)在A—G中互为同分异构体的是 (填写编号)。
(4)A的一种同分异构体H,它能发生银镜反应,但不能发生水解反应。写出H与银氨溶液反应的化学方程式 。
有机物A的结构简式为 ,它可通过不同的反应生成下列物质:
,它可通过不同的反应生成下列物质:
(1)在A—G中,不属于酯类的化合物有 (填写编号)。
(2)写出苯环上只有一个取代基,且组成上比A少一个碳原子的A的同系物的结构简式 。
(3)在A—G中互为同分异构体的是 (填写编号)。
(4)A的一种同分异构体H,它能发生银镜反应,但不能发生水解反应。写出H与银氨溶液反应的化学方程式 。