金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示。 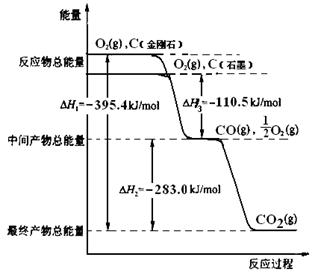
⑴、等量金刚石和石墨完全燃烧 ▲ (填“金刚石”或“石墨”)放出热量更多,表示石墨燃烧热的热化学方程式 ▲ 。
⑵、在通常状况下,金刚石和石墨 ▲ (填“金刚石”或“石墨”)更稳定,写出石
墨转化为金刚石的热化学方程式 ▲ 。
⑶、12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量 ▲ 。
金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示。 
⑴、等量金刚石和石墨完全燃烧 ▲ (填“金刚石”或“石墨”)放出热量更多,表示石墨燃烧热的热化学方程式 ▲ 。
⑵、在通常状况下,金刚石和石墨 ▲ (填“金刚石”或“石墨”)更稳定,写出石
墨转化为金刚石的热化学方程式 ▲ 。
⑶、12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量 ▲ 。