下图中,B、D、E、F、G是氧化物,F、K是氢化物,C、H是日常生活中最常见的金属单质,J是气态非金属单质。O是白色沉淀且B、H、L、M、N、O中含有同种元素,I是基础化学工业的重要产品(图中部分反应物和生成物没有列出)。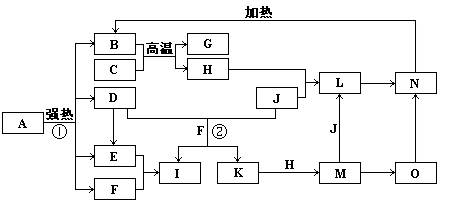
请按要求回答:
⑴、H元素在周期表中的位置 ▲ 。
⑵、写出G、L的化学式G: ▲ ,L: ▲ 。
⑶、反应②的离子方程式 ▲ 。
⑷、反应①是分解反应,反应中生成的B、D、E、F的物质的量之比为1∶1∶1∶14,则反应①的化学方程式为 ▲ 。
下图中,B、D、E、F、G是氧化物,F、K是氢化物,C、H是日常生活中最常见的金属单质,J是气态非金属单质。O是白色沉淀且B、H、L、M、N、O中含有同种元素,I是基础化学工业的重要产品(图中部分反应物和生成物没有列出)。
请按要求回答:
⑴、H元素在周期表中的位置 ▲ 。
⑵、写出G、L的化学式G: ▲ ,L: ▲ 。
⑶、反应②的离子方程式 ▲ 。
⑷、反应①是分解反应,反应中生成的B、D、E、F的物质的量之比为1∶1∶1∶14,则反应①的化学方程式为 ▲ 。