已知几种难溶电解质的溶度积如下表所示:
| 几种难溶电解质的Ksp(25℃) |
|
| 沉淀溶解平衡 |
Ksp |
 AgBr(s) Ag+(aq)+Br-(aq) AgBr(s) Ag+(aq)+Br-(aq) |
5,0×10-13mol2·L-2 |
 AgI(s) Ag+(aq)+I-(aq) AgI(s) Ag+(aq)+I-(aq) |
8.3×10-17mol2·L-2 |
 FeS(s) Fe2+(aq)+S2-(aq) FeS(s) Fe2+(aq)+S2-(aq) |
6.3×10-18mol2·L-2 |
 ZnS(s) Zn2+(aq)+S2-(aq) ZnS(s) Zn2+(aq)+S2-(aq) |
1.6×10-24mol2·L-2 |
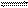 CuS(s) Cu2+(aq)+S2-(aq) CuS(s) Cu2+(aq)+S2-(aq) |
1.3×10-36mol2·L-2 |
(1)AgBr、AgI、FeS、ZnS、CuS的溶解能力由大到小的顺序为: 。
(2)向饱和的AgI溶液中加入固体硝酸银,则[I-] (填“增大”、“减小”或“不变”),若改加AgBr固体,则[Ag+] (填“增大”、“减小”或“不变”)。
(3)在25℃时,向100mL浓度均为0.1 mol·L-1 FeCl2、ZnCl2、CuCl2的混合溶液中逐滴加入Na2S溶液,生成的沉淀的先后顺序是 (用沉淀物的化学式表示)。
(4)在25℃时,把ZnS加入蒸馏水中,一定时间后达到如下平衡:
ZnS(s)  Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是( )
Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是( )
| A.加入少量CuS固体 | B.加入少量FeS固体 |
| C.加入少量FeCl2固体 | D.加入少量CuCl2固体 |
 +Na2CO3 = 2CH3COONa+CO2↑+H2O依照该规律,请判断下列反应不能成立的是___________(填编号)。
+Na2CO3 = 2CH3COONa+CO2↑+H2O依照该规律,请判断下列反应不能成立的是___________(填编号)。 ClO
ClO NaHCO3+C6H5OH
NaHCO3+C6H5OH +H2O +2C6H5ONa
+H2O +2C6H5ONa NaHCO3+C6H5ONa F.CH3COOH+NaCN = CH3COONa+HCN
NaHCO3+C6H5ONa F.CH3COOH+NaCN = CH3COONa+HCN 律。下列转化都属于复分解反应:
律。下列转化都属于复分解反应:
 。
。 与其气态氢化物反应得到离子化合物D。
与其气态氢化物反应得到离子化合物D。 [B(OH)4] –(aq)+H+(aq)K=5.7×10–10(298K)
[B(OH)4] –(aq)+H+(aq)K=5.7×10–10(298K) 粤公网安备 44130202000953号
粤公网安备 44130202000953号