Ⅰ.下列说法中正确的是。
| A.SO2和O3、PO43-和ClO4-互为等电子体 |
| B.甲烷分子失去一个H+,形成CH3-,其碳原子的杂化类型发生了改变 |
| C.Ti原子的核外电子排布式为[Ar]3d34s2 |
| D.CS2、H2O、C2H2都是直线形分子 |
E.CH4、BCl3、CO2都是含有极性键的非极性分子
Ⅱ.立方氮化硼是一种自然界不存在的人工合成超硬材料,硬度仅次于金刚石,是超硬材料领域的最重要成就之一。请回答下列问题:
(1)在第二周期,原子的第一电离能一般随核电荷数的增大而逐渐,比较下列原子的第一电离能:BeB,NO(填“>”“<”),其原因是。
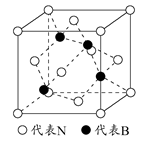
(2)如图为立方氮化硼的晶胞,则氮化硼的化学式为,该晶体中B原子填充N原子的空隙。若该晶胞的边长为a cm,那么该晶体的密度为g/cm3(只要求列出算式)。
(3)立方氮化硼的晶体结构与金刚石的结构相似,但其熔点比金刚石的低,试分析其原因:。
(4)立方氮化硼由六方氮化硼在高温高压下制备,六方氮化硼又称“白石墨”,结构和许多性质与石墨相似,六方氮化硼中N原子的杂化轨道类型为,请画出六方氮化硼的平面结构示意图(用“○”代表N原子,用“●”代表B原子,每种原子不少于7个)。