下图表示绿色植物细胞内部分物质的转化过程,1-5为反应过程,①-③为物质,请据图回答下列问题: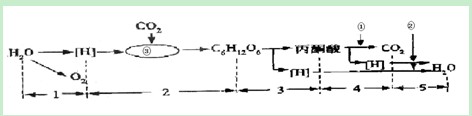
(1)图中①③代表的物质依次是 、 。
(2)图中只能在有光的条件下进行的过程是 ,过程2、3发生的场所依次是 、 。
(3)卡尔文用14C标记的14CO2,最终14CO2中的碳转化为葡萄糖中的碳,这一途径称为 。
(4)图中1、3、4过程产生的[H] (填“是”与“否”)都能与氧结合产生水?
下图表示绿色植物细胞内部分物质的转化过程,1-5为反应过程,①-③为物质,请据图回答下列问题:
(1)图中①③代表的物质依次是 、 。
(2)图中只能在有光的条件下进行的过程是 ,过程2、3发生的场所依次是 、 。
(3)卡尔文用14C标记的14CO2,最终14CO2中的碳转化为葡萄糖中的碳,这一途径称为 。
(4)图中1、3、4过程产生的[H] (填“是”与“否”)都能与氧结合产生水?