(每空3分,共15分)根据下框图关系,完成下列问题: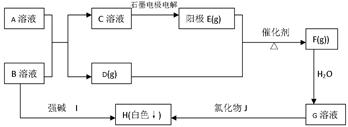
H(白色↓)不溶于盐酸,A、B都是酸式盐。
(1)工业生产D的典型设备是 ,工业生产F选择的条件是
(2)石墨电极电解C溶液时阳极的电极方程式是
(3)B溶液中加入I溶液反应恰好显中性时的离子方程式为
(4)B溶液与A溶液反应的离子方程式为
(每空3分,共15分)根据下框图关系,完成下列问题:
H(白色↓)不溶于盐酸,A、B都是酸式盐。
(1)工业生产D的典型设备是 ,工业生产F选择的条件是
(2)石墨电极电解C溶液时阳极的电极方程式是
(3)B溶液中加入I溶液反应恰好显中性时的离子方程式为
(4)B溶液与A溶液反应的离子方程式为