将下列物质进行分类:①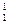 H与
H与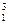 H ②O2与O3 ③
H ②O2与O3 ③ 乙醇与甲醚(CH3—O—CH3)④H2O与D2O ⑤CH3CH2CH2CH2
乙醇与甲醚(CH3—O—CH3)④H2O与D2O ⑤CH3CH2CH2CH2 CH3与CH3-CH(CH3)-CH3 ⑥C60与C70
CH3与CH3-CH(CH3)-CH3 ⑥C60与C70
(1)互为同位素的是 (填编号、下同);
(2)互为同素异形体的是 ;
(3)互为同分异构体的是 ;
(4)互为同系物的是 。
将下列物质进行分类:①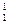 H与
H与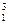 H ②O2与O3 ③
H ②O2与O3 ③ 乙醇与甲醚(CH3—O—CH3)④H2O与D2O ⑤CH3CH2CH2CH2
乙醇与甲醚(CH3—O—CH3)④H2O与D2O ⑤CH3CH2CH2CH2 CH3与CH3-CH(CH3)-CH3 ⑥C60与C70
CH3与CH3-CH(CH3)-CH3 ⑥C60与C70
(1)互为同位素的是 (填编号、下同);
(2)互为同素异形体的是 ;
(3)互为同分异构体的是 ;
(4)互为同系物的是 。