某有机化合物()与另一有机化合物发生如下反应生成化合物():
+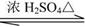 +
+
(1)是下列化合物之一,已知不能与溶液发生显色反应。则是(填标号字母)。
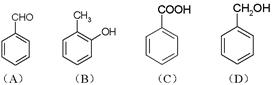
(2)的分子式是,可能的结构简式是:和。
(3)有多种同分异构体,其中一种同分异构体发生银镜反应后,其产物经酸化可得()。可发生如下反应:
F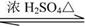
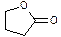 +该反应的类型是,的结构简式是。
+该反应的类型是,的结构简式是。
(4)若与具有相同的碳链,则的结构简式为:。
某有机化合物()与另一有机化合物发生如下反应生成化合物():
+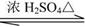 +
+
(1)是下列化合物之一,已知不能与溶液发生显色反应。则是(填标号字母)。

(2)的分子式是,可能的结构简式是:和。
(3)有多种同分异构体,其中一种同分异构体发生银镜反应后,其产物经酸化可得()。可发生如下反应:
F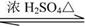
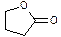 +该反应的类型是,的结构简式是。
+该反应的类型是,的结构简式是。
(4)若与具有相同的碳链,则的结构简式为:。