(12分)右图是铜锌原电池装置。其电池的总反应是:
Zn(s) + CuSO4(aq)="=" ZnSO4(aq) + Cu(s)。
请回答以下问题: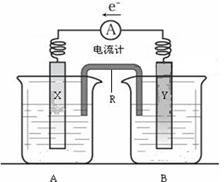
(1)R的名称是__________________,R中的阳离子移向_______(填A或B)中的溶液。
(2)电极Y的材料是________,B中的电解质溶液是________________。
(3)X为原电池的______极,其电极反应式是____________________________。
(12分)右图是铜锌原电池装置。其电池的总反应是:
Zn(s) + CuSO4(aq)="=" ZnSO4(aq) + Cu(s)。
请回答以下问题:
(1)R的名称是__________________,R中的阳离子移向_______(填A或B)中的溶液。
(2)电极Y的材料是________,B中的电解质溶液是________________。
(3)X为原电池的______极,其电极反应式是____________________________。