某离子晶体晶胞如图所示,阳离子 X(●)位于立方体的顶点,阴离子Y(○)位于立方体的中心,试分析: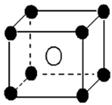
(1)晶体中Y的配位数是 ; X的配位数是 ;该晶体的化学式为 。
(2)晶体中在每个X周围与它最接近且距离相等的X共有 个。
(3)该晶体的摩尔质量为M g/mol,晶体密度为ρ g/cm3,阿伏加德罗常数为NA,则晶体中两个距离最近的X中心间的距离为 cm。
某离子晶体晶胞如图所示,阳离子 X(●)位于立方体的顶点,阴离子Y(○)位于立方体的中心,试分析:
(1)晶体中Y的配位数是 ; X的配位数是 ;该晶体的化学式为 。
(2)晶体中在每个X周围与它最接近且距离相等的X共有 个。
(3)该晶体的摩尔质量为M g/mol,晶体密度为ρ g/cm3,阿伏加德罗常数为NA,则晶体中两个距离最近的X中心间的距离为 cm。