将2.5g碳酸钠、碳酸氢钠和氢氧化钠固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol·L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示: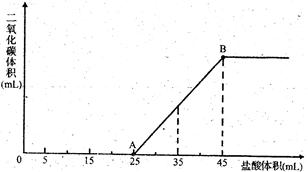
(1)写出OA段所发生反应的离子方程式: ;
(2)当加入35mL盐酸时,产生二氧化碳的体积为 mL(标准状况);
(3)原混合物中Na2CO3的质量分数为 。
将2.5g碳酸钠、碳酸氢钠和氢氧化钠固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol·L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
(1)写出OA段所发生反应的离子方程式: ;
(2)当加入35mL盐酸时,产生二氧化碳的体积为 mL(标准状况);
(3)原混合物中Na2CO3的质量分数为 。