铁氧体(Fe3O4)法是处理含铬废水的常用方法。其原理是用FeSO4把废水中Cr2O72-离子还原为Cr3+离子,并通过调节废水pH,使生成物组成符合类似于铁氧体(Fe3O4或FeO·Fe2O3)的复合氧化物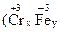 ·
·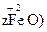 。若处理含1 mol Cr2O72-的废水至少需要加入10mol FeSO4·7H2O,则
。若处理含1 mol Cr2O72-的废水至少需要加入10mol FeSO4·7H2O,则
| A.x=1,y=4,z=6 | B.x=0.5,y=1.5,z=8.5 |
| C.x=2,y=4,z=6 | D.x=2,y=6,z=4 |
铁氧体(Fe3O4)法是处理含铬废水的常用方法。其原理是用FeSO4把废水中Cr2O72-离子还原为Cr3+离子,并通过调节废水pH,使生成物组成符合类似于铁氧体(Fe3O4或FeO·Fe2O3)的复合氧化物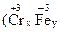 ·
·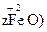 。若处理含1 mol Cr2O72-的废水至少需要加入10mol FeSO4·7H2O,则
。若处理含1 mol Cr2O72-的废水至少需要加入10mol FeSO4·7H2O,则
| A.x=1,y=4,z=6 | B.x=0.5,y=1.5,z=8.5 |
| C.x=2,y=4,z=6 | D.x=2,y=6,z=4 |