某化学兴趣小组为探究的性质,按下图所示装置进行实验。
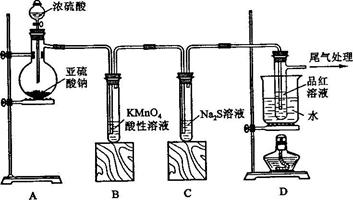
请到答列问题:
(1)装置中盛放亚硫酸钠的仪器名称是,其中发生反 应的化学方程式为;
应的化学方程式为;
(2)实验过程中,装置、中发生的现象分别是、,这些现象分别说明具有的性质是和;装置B中发生反应的离子方程式为;
(3)装置的目的是探究与品红作用的可逆性,请写出实验操作及象;
(4)尾气可采用 溶液吸收。
溶液吸收。
某化学兴趣小组为探究的性质,按下图所示装置进行实验。

请到答列问题:
(1)装置中盛放亚硫酸钠的仪器名称是,其中发生反 应的化学方程式为;
应的化学方程式为;
(2)实验过程中,装置、中发生的现象分别是、,这些现象分别说明具有的性质是和;装置B中发生反应的离子方程式为;
(3)装置的目的是探究与品红作用的可逆性,请写出实验操作及象;
(4)尾气可采用 溶液吸收。
溶液吸收。