有机物的结构可用“键线式”简化表示,如:CH3-CH=CH-CH3可表示为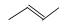 ,有一种有机物X它的键线式如下:
,有一种有机物X它的键线式如下: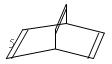
(1)X的分子式为: ;有机物Y是X的同分异构体,且属于芳香族
化合物。则Y的结构简式是 。
(2)Y可以与溴水反应,其生成物的结构简式是 ; Y在一定条件下
还可生成高分子化合物,写出该反应的化学方程式 。
有机物的结构可用“键线式”简化表示,如:CH3-CH=CH-CH3可表示为 ,有一种有机物X它的键线式如下:
,有一种有机物X它的键线式如下:
(1)X的分子式为: ;有机物Y是X的同分异构体,且属于芳香族
化合物。则Y的结构简式是 。
(2)Y可以与溴水反应,其生成物的结构简式是 ; Y在一定条件下
还可生成高分子化合物,写出该反应的化学方程式 。