某校化学研究学习小组设计如下实验方案,测定放置已久的小苏打样品中纯碱的质量分数。按右图装置进行实验,已知B中盛放的是浓硫酸。并回答以下问题。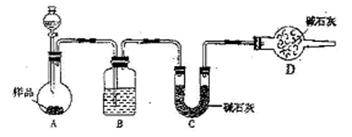
(1)实验加入药品前应先 。分液漏中应该装 (填:盐酸或硫酸)。
D装置的作用是 。
(2)实验中除称量样品质量外,还需称 装置前后质量的变化。
某校化学研究学习小组设计如下实验方案,测定放置已久的小苏打样品中纯碱的质量分数。按右图装置进行实验,已知B中盛放的是浓硫酸。并回答以下问题。
(1)实验加入药品前应先 。分液漏中应该装 (填:盐酸或硫酸)。
D装置的作用是 。
(2)实验中除称量样品质量外,还需称 装置前后质量的变化。