金晶体的最小重复单元(也称晶胞)是面心立方体,即在立方体的8个顶点上各有一个金原子,各个面的中心有一个金原子,每个金原子被相邻的晶胞所共有(见图1-25)。金原子的直径为d,用NA表示阿伏加德罗常数,M表示金的摩尔质量。
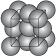
图1-25
(1)金晶体每个晶胞中含有 个金原子。
(2)欲计算一个晶胞的体积,除假定金属原子是刚性小球外,还应假定 。
(3)一个晶胞的体积是 。
(4)金晶体的密度是 。
金晶体的最小重复单元(也称晶胞)是面心立方体,即在立方体的8个顶点上各有一个金原子,各个面的中心有一个金原子,每个金原子被相邻的晶胞所共有(见图1-25)。金原子的直径为d,用NA表示阿伏加德罗常数,M表示金的摩尔质量。

图1-25
(1)金晶体每个晶胞中含有 个金原子。
(2)欲计算一个晶胞的体积,除假定金属原子是刚性小球外,还应假定 。
(3)一个晶胞的体积是 。
(4)金晶体的密度是 。