已知T℃、p kPa时,往容积可变的密闭容器中充入2 mol X和1 mol Y,此时容积为VL。保持恒温恒压,发生反应:2X(气)+Y(气)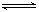 2Z(气),达到平衡时,平衡气中Z的体积分数为0.4。试回答下列有关问题:
2Z(气),达到平衡时,平衡气中Z的体积分数为0.4。试回答下列有关问题:
(1)使温度和压强在上述条件下恒定不变,再往上述密闭容器内充入4molZ,则反应达到平衡时,容器的容积为,平衡气中Z的体积分数为。
(2)若另选一个容积固定不变的密闭容器,仍控制温度为T℃,使3molX和1.5molY反应,达到平衡状态时,平衡气中Z的体积分数仍为0.4,则该密闭容器的容积为。