A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两种元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等。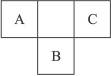
(1)写出A、B、C三元素的名称:A是__________,B是__________,C是__________。
(2)B、C两元素可形成BC6型化合物,该化合物(填“能”或“不能”)燃烧,其理由是______________________________________________________________________________。
A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两种元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等。
(1)写出A、B、C三元素的名称:A是__________,B是__________,C是__________。
(2)B、C两元素可形成BC6型化合物,该化合物(填“能”或“不能”)燃烧,其理由是______________________________________________________________________________。