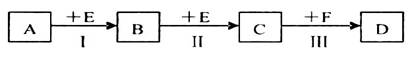
已知:①A、B、C、D四种物质均含元素X,有的还可能含有元素Y、Z。元素Y、X、Z的原子序数依次递增 ②X在A、B、C、D中都不呈现它的最高化合价 ③室温下单质A与某种常见一元强碱溶液反应,可得到B和C ④化合物D受热催化分解,可制得元素Y的单质。
(1)元素X是__________________________,Z是__________________________。
(2)写出③中反应的化学方程式:_______________________________。
(3)写出④中反应的化学方程式:______________________________。
 SO3(g)+NO(g)
SO3(g)+NO(g)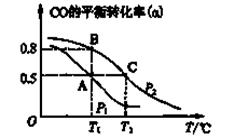
 mol
mol ,则:
,则: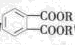 (其中R为烃基)。实验室由以下方法可得到DMP:
(其中R为烃基)。实验室由以下方法可得到DMP:
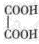 )在一定条件下可以按物质的量1:1发生反应生成高分子化合物,反应的化学方程式为。
)在一定条件下可以按物质的量1:1发生反应生成高分子化合物,反应的化学方程式为。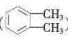 )为原料先生产苯酐
)为原料先生产苯酐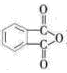 ),再使其与某醇在一定条件下反应制取DMP。苯酐与该醇制取DMP的化学方程式为。
),再使其与某醇在一定条件下反应制取DMP。苯酐与该醇制取DMP的化学方程式为。
 衡量过碳酸钠产品的优势,13%以上为优等品。取2g某厂家生产的过碳酸钠样品(所含杂质不参加反应)溶于水配成溶液,加入足量MnO2,反应完全后溶液质量减轻0.264g,则该样品中活性氧的质量分数为 。
衡量过碳酸钠产品的优势,13%以上为优等品。取2g某厂家生产的过碳酸钠样品(所含杂质不参加反应)溶于水配成溶液,加入足量MnO2,反应完全后溶液质量减轻0.264g,则该样品中活性氧的质量分数为 。 粤公网安备 44130202000953号
粤公网安备 44130202000953号