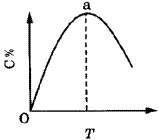
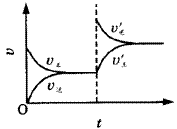
图1表示mA(g)+nB(g) pC(g)+qD(g)+Q,在不同温度下经过一定时间混合体系中C的质量分数与温度T的关系;图2表示在一定条件下达到平衡(v正=v逆)后t时刻改变影响平衡的另一个条件重新建立新平衡的反应过程,判断该反应是( )。
pC(g)+qD(g)+Q,在不同温度下经过一定时间混合体系中C的质量分数与温度T的关系;图2表示在一定条件下达到平衡(v正=v逆)后t时刻改变影响平衡的另一个条件重新建立新平衡的反应过程,判断该反应是( )。
 |
 |
| 图1 曲线图 |
图2 曲线图 |
| A.m+n>p+qQ>0 |
| B.m+n>p+qQ<0 |
| C.m+n<p+qQ>0 |
| D.m+n<p+qQ<0 |
图1表示mA(g)+nB(g) pC(g)+qD(g)+Q,在不同温度下经过一定时间混合体系中C的质量分数与温度T的关系;图2表示在一定条件下达到平衡(v正=v逆)后t时刻改变影响平衡的另一个条件重新建立新平衡的反应过程,判断该反应是( )。
pC(g)+qD(g)+Q,在不同温度下经过一定时间混合体系中C的质量分数与温度T的关系;图2表示在一定条件下达到平衡(v正=v逆)后t时刻改变影响平衡的另一个条件重新建立新平衡的反应过程,判断该反应是( )。
 |
 |
| 图1 曲线图 |
图2 曲线图 |
| A.m+n>p+qQ>0 |
| B.m+n>p+qQ<0 |
| C.m+n<p+qQ>0 |
| D.m+n<p+qQ<0 |