已知NH3和Cl2可快速反应:2NH3+3Cl2====N2+6HCl
图1-6为反应后总体积V(L)随原混合气体中Cl2的体积分数(x%)而变化的曲线。试计算: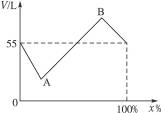
图1-6
(1)当反应结束后处于A、B两点时,原混合气体中Cl2的体积分数各是多少?
(2)当反应结束时处于A、B两点,混合气体的总体积各是多少升?
(3)若反应结束时气体总体积为11 L,求原混合物中Cl2的体积分数。
已知NH3和Cl2可快速反应:2NH3+3Cl2====N2+6HCl
图1-6为反应后总体积V(L)随原混合气体中Cl2的体积分数(x%)而变化的曲线。试计算:
图1-6
(1)当反应结束后处于A、B两点时,原混合气体中Cl2的体积分数各是多少?
(2)当反应结束时处于A、B两点,混合气体的总体积各是多少升?
(3)若反应结束时气体总体积为11 L,求原混合物中Cl2的体积分数。