图示表示800℃时A、B、C三种气体物质的浓度随时间的变化情况,t1是到达平衡状态的时间.试回答: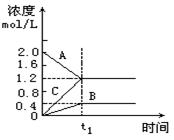
(1)该反应的反应物是____ __;
(2)反应物的转化率是____ __;
(3)该反应的化学方程式为___ ___.
图示表示800℃时A、B、C三种气体物质的浓度随时间的变化情况,t1是到达平衡状态的时间.试回答:
(1)该反应的反应物是____ __;
(2)反应物的转化率是____ __;
(3)该反应的化学方程式为___ ___.