根据下图所示实验,填空和回答问题。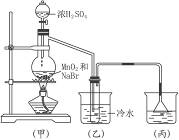
(1)烧瓶中所发生的主要反应的化学方程式是___________;装置(乙)的烧杯中冷水所起的作用是___________;装置(丙)的烧杯中液体的作用是___________。
(2)进行此实验时,烧杯内的橡皮塞最好用铝箔包住,用橡皮管连接的两玻璃管口要相互紧靠,这是因为___________,装置(丙)的烧杯中使用倒置漏斗可防止液体倒吸,其原因是___________。
根据下图所示实验,填空和回答问题。
(1)烧瓶中所发生的主要反应的化学方程式是___________;装置(乙)的烧杯中冷水所起的作用是___________;装置(丙)的烧杯中液体的作用是___________。
(2)进行此实验时,烧杯内的橡皮塞最好用铝箔包住,用橡皮管连接的两玻璃管口要相互紧靠,这是因为___________,装置(丙)的烧杯中使用倒置漏斗可防止液体倒吸,其原因是___________。