常温下,两种常见无色无味的气体A和B组成的混合气体(A的相对分子质量小于B的相对分子质量)。经分析混合气体中总共只含氧和碳两种元素,但不论A和B以何种比例混合,氧和碳的质量比总是大于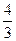 。
。
(1)在下表中填出A和B可能的分子式。(不一定填满)
(2)当氧和碳的质量比等于2时,试确定A和B的可能组成以及A与B的物质的量之比。
常温下,两种常见无色无味的气体A和B组成的混合气体(A的相对分子质量小于B的相对分子质量)。经分析混合气体中总共只含氧和碳两种元素,但不论A和B以何种比例混合,氧和碳的质量比总是大于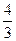 。
。
(1)在下表中填出A和B可能的分子式。(不一定填满)
(2)当氧和碳的质量比等于2时,试确定A和B的可能组成以及A与B的物质的量之比。