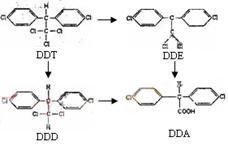
⑴分子中所有原子可以处于同一平面的有 (选填“DDT、DDE、DDD、 DDA”)。
⑵DDA中所含的官能团,除苯环外,还有
⑶指出下列有机反应类型:①DDT→DDE 反应;②DDE→DDD 反应
⑷若在实验室也可实现由DDT→—DDE,试写出该反应的化学方程式:

⑴分子中所有原子可以处于同一平面的有 (选填“DDT、DDE、DDD、 DDA”)。
⑵DDA中所含的官能团,除苯环外,还有
⑶指出下列有机反应类型:①DDT→DDE 反应;②DDE→DDD 反应
⑷若在实验室也可实现由DDT→—DDE,试写出该反应的化学方程式: