在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请完成下列问题: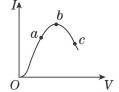
(1)“O”点导电能力为0的理由是____________。
(2)a、b、c三点处,溶液的c(H+)由小到大的顺序为____________。
(3)a、b、c三点处,电离程度最大的是____________。
(4)若使c点溶液中c(CH3COO-)增大,溶液c(H+)减小,可采取的措施是:①____________;②____________;③____________。
在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请完成下列问题:
(1)“O”点导电能力为0的理由是____________。
(2)a、b、c三点处,溶液的c(H+)由小到大的顺序为____________。
(3)a、b、c三点处,电离程度最大的是____________。
(4)若使c点溶液中c(CH3COO-)增大,溶液c(H+)减小,可采取的措施是:①____________;②____________;③____________。