已知任何化学反应都遵循电荷守恒和质量守恒。如下是单质铁溶于一定浓度的硝酸中反应的化学方程式:
aFe+b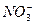 +cH+====dFe2++fFe3++gNO↑+hN2O↑+kH2O(化学计量数均为正整数)
+cH+====dFe2++fFe3++gNO↑+hN2O↑+kH2O(化学计量数均为正整数)
请你用已掌握的知识研究出下列规律:
(1)c、g、h的关系式是___________________;
(2)b、c、d、f的关系式是________________;
(3)d、f、g、h的关系式是______________。
已知任何化学反应都遵循电荷守恒和质量守恒。如下是单质铁溶于一定浓度的硝酸中反应的化学方程式:
aFe+b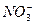 +cH+====dFe2++fFe3++gNO↑+hN2O↑+kH2O(化学计量数均为正整数)
+cH+====dFe2++fFe3++gNO↑+hN2O↑+kH2O(化学计量数均为正整数)
请你用已掌握的知识研究出下列规律:
(1)c、g、h的关系式是___________________;
(2)b、c、d、f的关系式是________________;
(3)d、f、g、h的关系式是______________。