已知:①通常Br2与“C=C”双键起加成反应,但高温下Br2易取代与“C=C”双键直接相连的α-碳原子上的氢原子:
②与苯环直接相连的支链碳原子上的氢原子也易被溴取代: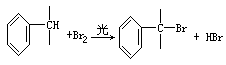
③卤代烃在一定条件下可以水解成醇:
卤代烃也可在一定条件下发生消去反应生成烯烃:
</PGN0069B.TXT/PGN>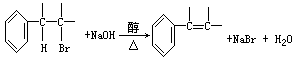
根据上述有关知识推断如何从正丙苯制取1-苯基丙三醇:C6H5—CHOH—CHOH—CH2OH,写出各步反应方程式(注明反应条件)。
已知:①通常Br2与“C=C”双键起加成反应,但高温下Br2易取代与“C=C”双键直接相连的α-碳原子上的氢原子:
②与苯环直接相连的支链碳原子上的氢原子也易被溴取代:
③卤代烃在一定条件下可以水解成醇:
卤代烃也可在一定条件下发生消去反应生成烯烃:
</PGN0069B.TXT/PGN>
根据上述有关知识推断如何从正丙苯制取1-苯基丙三醇:C6H5—CHOH—CHOH—CH2OH,写出各步反应方程式(注明反应条件)。