工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
①CO(g)+H2O(g)  CO2(g)+H2(g)△H=-41 kJ/mol
CO2(g)+H2(g)△H=-41 kJ/mol
某小组研究在相同温度下该反应过程中的能量变化。他们分别在体积均为VL的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应。相关数据如下:
容器编号
|
起始时各物质物质的量/mol
|
达到平衡的时间/min
|
达平衡时体系能量的变化/kJ
|
CO
|
H2O
|
CO2
|
H2
|
①
|
1
|
4
|
0
|
0
|
t1
|
放出热量:32.8 kJ
|
②
|
2
|
8
|
0
|
0
|
t2
|
放出热量:Q
|
|
|
|
|
|
|
|
|
(1)该反应过程中,反应物分子化学键断裂时所吸收的总能量(填“大于”、“小于”或“等于”)生成物分子化学键形成时所释放的总能量。
(2)容器①中反应达平衡时,CO的转化率为%。
(3)计算容器②中反应的平衡常数K=。
(4)下列叙述正确的是 (填字母序号)。
A.平衡时,两容器中H2的体积分数相等
B.容器②中反应达平衡状态时,Q > 65.6 kJ
C.反应开始时,两容器中反应的化学反应速率相等
D.容器①中,化学反应速率为: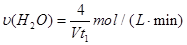
(5)已知:②2H2 (g) + O2 (g) = 2H2O (g)ΔH=-484 kJ/mol,写出CO完全燃烧生成CO2的热化学方程式:。
(6)容器①中反应进行到t min时,测得混合气体中CO2的物质的量为0.6 mol。若用200 mL 5 mol/L的NaOH溶液将其完全吸收,反应的离子方程式为(用一个离子方程式表示)。
(7)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用图中所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。
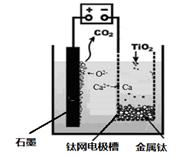
①写出阳极所发生反应的电极反应式:。
②在制备金属钛前后,CaO的总量不变,其原因是(请结合反应式解释)。