化学实验中的很多气体是用盐酸来制取的,这就导致了这些制取的气体中往往含有HCl杂质,要除去HCl杂质而得到纯净的目标气体,可用右图所示装置。如果广口瓶中盛装的是饱和NaHCO3溶液,则可以用于下列哪种气体的除杂装置是 ( )。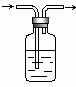
| A.H2 | B.Cl2 | C.H2S | D.CO2 |
化学实验中的很多气体是用盐酸来制取的,这就导致了这些制取的气体中往往含有HCl杂质,要除去HCl杂质而得到纯净的目标气体,可用右图所示装置。如果广口瓶中盛装的是饱和NaHCO3溶液,则可以用于下列哪种气体的除杂装置是 ( )。
| A.H2 | B.Cl2 | C.H2S | D.CO2 |