硫代硫酸钠(Na2S2O3)可看成是一个S原子取代了Na2SO4中的一个O原子而形成。某校化学研究性学习小组运用类比学习的思想,通过实验探究Na2S2O3的化学性质。
【提出问题】Na2S2O3是否与Na2SO4相似具备下列性质呢?
猜想①: ▲ ;
猜想②:溶液呈中性,且不与酸反应;
猜想③:无还原性,不能被氧化剂氧化。
【实验探究】基于上述猜想②、③,设计实验方案。
| |
实验操作 |
实验现象或 预期实验现象 |
现象解释 (用离子方程式表示) |
| 猜想② |
▲ |
溶液pH=8 |
— |
| 向pH=2的硫酸中滴加Na2S2O3溶液 |
▲ |
S2O32—+2H+=S↓+SO2↑+H2O |
|
| 猜想③ |
向新制氯水(pH<2)中滴加少量Na2S2O3溶液 |
氯水颜色变浅 |
▲ |
【实验结论】Na2S2O3能与酸反应,具有还原性,与Na2SO4的化学性质不相似。
【问题讨论】
⑴甲同学向探究“猜想③”反应后的溶液中滴加硝酸银溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化。你认为该方案是否正确并说明理由 ▲ 。
⑵请重新设计一个实验方案,证明Na2S2O3被氯水氧化。该实验方案是 ▲ 。
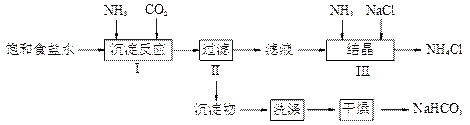
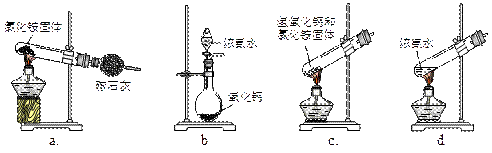
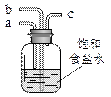
 作用是_________。
作用是_________。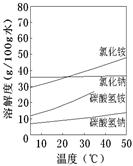
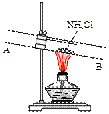

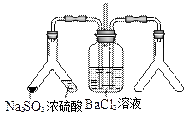
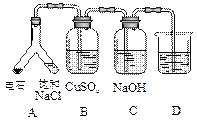
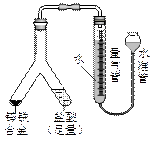
 ,则合金中铁的含量为________%(保留2位小数,已折算标况)。
,则合金中铁的含量为________%(保留2位小数,已折算标况)。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号