某化肥厂以氨和空气(其中氧气的体积分数为0.2)为原料生产硝酸铵过程如下: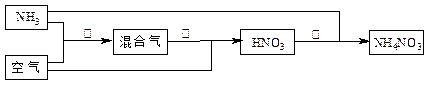
其中反应①为4NH3+5O2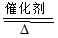 4NO+6H2O
4NO+6H2O
⑴步骤②中发生了两个反应,将这两个化学方程式合并为一个化学方程式,可表示为_____________
________________________。
⑵若不考虑副反应且各步反应均完全,为使生产过程中不再补充空气,则原料气中氨(包括第③步被硝酸吸收的氨)的体积分数最大值为____________。
⑶假设实际生产中,反应①、②中含氮物质的利用率分别为a、b,反应③中氨的利用率为c、硝酸的利用率为100%,则合成硝酸铵的整个流程中,氨的总利用率是多少?




 、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等。
、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等。

 。已知在一定压强下,该反应随温度的升高而CO2的转化率降低。则该反应的
。已知在一定压强下,该反应随温度的升高而CO2的转化率降低。则该反应的 ________ 0(填“ >”或“ <”);若用以甲醚、空气、氢氧化钾溶液为原料,石墨为电极构成燃料电池,则该电池中负极的电极反应式是________________________________,放电过程中溶液的PH________ (填“增大”、“减小”或“不变”)。
________ 0(填“ >”或“ <”);若用以甲醚、空气、氢氧化钾溶液为原料,石墨为电极构成燃料电池,则该电池中负极的电极反应式是________________________________,放电过程中溶液的PH________ (填“增大”、“减小”或“不变”)。
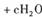 ,上述离子方程式可能的配平系数有多组。请回答:
,上述离子方程式可能的配平系数有多组。请回答: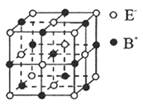
 粤公网安备 44130202000953号
粤公网安备 44130202000953号