有一硝酸钾溶液,其中混入少量KBr、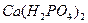 ,有人拟用
,有人拟用 、
、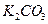 、KOH和
、KOH和 作试剂除去杂质,且最后溶液中只含
作试剂除去杂质,且最后溶液中只含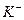 、
、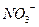 、
、 。
。
(1)加入试剂的顺序是: 。
(2)用离子方程式依次表示所发生的各化学反应
有一硝酸钾溶液,其中混入少量KBr、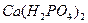 ,有人拟用
,有人拟用 、
、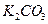 、KOH和
、KOH和 作试剂除去杂质,且最后溶液中只含
作试剂除去杂质,且最后溶液中只含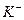 、
、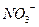 、
、 。
。
(1)加入试剂的顺序是: 。
(2)用离子方程式依次表示所发生的各化学反应