[江苏]2014年初中毕业升学考试(江苏南通卷)化学
未成年人正处于生长发育阶段,需要摄入比成年人更多的常量元素是( )
| A. | 钙 | B. | 硒 | C. | 碘 | D. | 锌 |
粗盐提纯需经过称量、溶解、过滤、蒸发等操作,下列图示对应的操作不规范的是( )
| A. |
称量

|
B. |
溶解

|
C. |
过滤

|
D. |
蒸发

|
水是最常见的物质。以下与水有关的说法正确的是
下列实验中,仪器和用品的选择不合理的是()

| A. | 收集 气体--⑥⑦⑧ |
| B. | 检验一瓶气体是否为 -⑦⑧⑨ |
| C. | 用 溶液和 制 --①② |
| D. | 用大理石和稀盐酸制 --③④⑤ |
下列有关物质性质与用途的说法均正确的是()
| A. | 一氧化碳具有还原性,可用于铁的冶炼 |
| B. | 金属铝不能与氧气反应,常用于制作炊具 |
| C. | 碳酸钠能与酸反应,常用于治疗胃酸过多 |
| D. | 活性炭具有吸附性,常用于自来水杀菌消毒 |
盐场晒盐后得到的卤水中含有
和
等物质,它们的溶解度曲线如下图所示.下列说法正确的是

根据下列实验现象不能判断有新物质生成的是
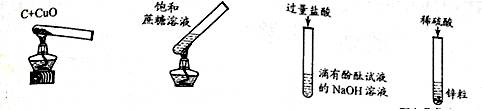
下列说法正确的是
| A. | 用紫色石蕊试液可以区分氢氧化钠溶液和澄清石灰水 |
| B. | 用适量 溶液可除去 溶液中混有的 |
| C. | 将铁钉分别置于干燥、潮湿的空气中,可探究水对铁生锈的影响 |
| D. | 配制一定溶质质量分数的稀硫酸时,应将水倒入浓硫酸中稀释 |
地球大气的演化经历了原始大气、次生大气和现代大气三个阶段,次生大气中部分成分的微观示意图如下:
| 甲 |
乙 |
丙 |
 |
 |
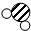 |
 |
一定条件下,3.4g甲物质和4.8g氧气恰好完全反应,生成5.4g乙物质和另一种物质
,下列判断不正确的是
物质甲的化学式是
物质 的质量为2.8g
物质 中含两种元素
该反应化学方程式中物质 与 的化学计量数之比为2:3
了解物质的组成和结构,有助于认识物质的性质。
(1)下图表示核电荷数为11~17的元素最高和最低化合价。

①从图中可以看出,氯元素的最高正价是。
②若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为。
③写出图中元素的化合价随着核电荷数递增的一条变化规律。
(2)在金属活动性顺序表里,通常排在前面的金属更易失去电子。回答以下问题:
①某金属原子的结构示意图为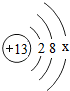 ,则最外层电子数x=;若最外层电子失去,达到相对稳定结构,该带电粒子的符号为。
,则最外层电子数x=;若最外层电子失去,达到相对稳定结构,该带电粒子的符号为。
②我国古代发明了"曾青(即硫酸铜)得铁化为铜"的湿法炼铜法,请用化学方程式表示反应原理;反反应中,更易失去电子的金属是。
七水硫酸镁(MgSO4·7H2O)是一种重要的化工原料,在48.1℃以下的潮湿空气中稳定,在温热干燥空气中易失去结晶水。工业上将白云石(主要成分为MgCO3、CaCO3)煅烧成粉,用于制取MgSO4·7H2O,工艺流程如下图所示:

(1)煅烧过程中,MgCO3转化为MgO的基本反应类型是。
(2)写出MgO与H2SO4反应的化学方程式。
(3)操作a的名称为。
(4)将分离后的母液循环利用的目的是。
(5)干燥得成品时,需要控制的条件是。
空气是一种宝贵的自然资源,要保护空气,防止污染空气。
(1)分离液化空气可获得氮气和
(2)利用膜分离技术,在一定压力下让空气通过具有富集氧气功能的薄膜,能得到含氧量较高的富氧空气,该过程发生
(3)某燃煤电厂富氧燃烧技术原理图如下:

①富氧燃烧与普通燃烧相比,能提供更多的
,使锅炉中的
充分燃烧,请写出
燃烧的化学方程式
②采用该技术有利于对
捕捉、封存和利用,减少碳排放,获得的
可用于制干冰,干冰的用途之一是
③采用图中工艺,可以使煤燃烧产生的氮氧化物和
实验室使用块状石灰石(
)和稀盐酸制
,当观察不到有气泡产生,固体仍有剩余时,通常认为反应结束,剩余液呈中性。某兴趣小组对此进行了以下探究:
【实验操作】(1)向试管中加入5粒石灰石,倾倒约试管体积1/3的稀盐酸(1:1);观察不到气泡后,仍有固体剩余;将试管静置。
(2)取上层清液,用pH试纸测得溶液pH=2,说明溶液显
pH测定中,"上层清液滴到试纸上"的后一步操作是
【实验思考Ⅰ】反应剩余液中有哪些物质?其中能使溶液pH=2的有哪些?
【实验探究Ⅰ】(1)甲同学通过实验排除了
的可能性。简述其实验方案
(2)乙同学将
通入蒸馏水中至饱和,测得pH>5,。
(3)综合甲、乙两同学实验,得出的结论是:剩余液中还含有
【实验思考Ⅱ】试管中剩余固体是否仍含有
?
【实验探究Ⅱ】小组同学向试管中继续加入稀盐酸(1:1),又有大量气泡产生。
(1)由此得出的结论是
(2)比较稀盐酸加入前后的实验现象,解释"又有大量气泡产生"的原因:
【拓展延伸】(1)反应剩余液放置一段时间后,溶液pH增大,其主要原因是
(2)假如用100g14.6%的稀盐酸和足量的石灰石反应,看不到气泡产生时,停止收集气体。收集到的
质量
一定条件下,糖类(按
计,相对分子质量为
)发酵生成乙醇(
),也可发酵生成乙酸(
)。
(1)
中
、
、
三种元素的质量比为
(2)某调味剂厂采用发酵技术生产的"原醋"中,乙酸的质量分数为
,将
上述"原醋"稀释成质量分数为
的食醋,需水的质量为
(3)糖类发酵生成乙醇的化学方程式为:
(反应条件省略,下同)
①求
上述糖理论上制得乙醇的质量。(请将计算过程写到答题卡上)
②糖类和乙醇在空气中燃烧的化学方程式分别为:
已知完全燃烧
上述糖生产
的水,若将①中制得的乙醇完全燃烧,则生成水的质量为
 粤公网安备 44130202000953号
粤公网安备 44130202000953号