[福建]2014年初中毕业升学考试(福建龙岩卷)化学
氧化铟锡是触摸屏技术重要材料,它由氧化锡和氧化铟熔融而成。氧化铟( )中,铟元素( )的化合价为
| A. | 0 | B. | B | C. | D. |
下列有关物质应用的叙述,错误的是
近期我国部分地区发生洪涝灾害,饮用水源受到污染。为保证居民正常生活,必须对饮用水源净化处理。若用下述方法处理饮用水源:①消毒②自然沉降③过滤,处理先后顺序是()
| A. | ②③① | B. | ②①③ | C. | ③②① | D. | ③①② |
维生素C( )是人体不可缺少的营养物质。下列说法错误的是()
| A. | 维生素C不属于氧化物 | B. | 维生素C 中碳、氧元素质量比为1:1 |
| C. | 维生素C能增强人体抗病能力 | D. | 新鲜水果和蔬菜中富含维生素C |
、 和 都是身边常见的物质。下列说法正确的是()
| A. | 能支持燃烧,可用作燃料 |
| B. | 由氢分子和氧原子构成 |
| C. | 可用带火星的木条鉴别 和 |
| D. | 是光合作用的原料,空气中含量越高越好 |
下列事实与对应的解释不相符的是
分解需吸收热量,生成耐高温的 和水蒸气。利用这一性质,可将 添加到易燃性材料中做阻燃剂。关于 能起阻燃作用的叙述,错误的是
| A. | 分解要吸热,降低了可燃物的着火点 |
| B. | 分解能够降温,使可燃物不易达到着火点 |
| C. | 分解生成的 覆盖在可燃物表面,隔绝了空气 |
| D. | 分解生成大量水蒸气,降低可燃物周围氧气的浓度 |
"接龙"是化学扑克(和普通扑克相似,牌面标注物质的化学式)的一种游戏,其规则是:当上家出牌时,下家跟出的牌所标注的物质必须能与上家的反应。某局游戏中,甲到戊五人各有一张不同的牌,牌面标注" "、" "、" "、" "、" "。若甲的牌为" ",且按甲-乙-丙-丁-戊依次出牌时能满足"接龙"规则,则丁的牌是
| A. | B. | C. | D. |
下图为硫酸钠和氯化钠的溶解度曲线。下列说法正确的是

下图是燃气热水器示意图。

(1)某热水器以天然气(主要成分是
)为燃气。
①写出
完全燃烧的化学方程式:;
②当"空气进气孔"被部分堵塞,燃烧将产生有毒气体
。
的化学式为。
(2)1
不同燃料燃烧产生
和
的质量如表。

①最不会污染环境的燃料是;
②燃烧时最会促成酸雨的燃料是。
化学是在原子、分子水平上研究物质及其变化的科学。
(1)现有下列化学式或微粒符号:①
、②
、③
、④
。其中,"2"表示2个分子的是
(2)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如下。下列说法正确的是

反应前后共有4种原子
该反应有单质生成
反应前后元素化合价都不变
化学变化中分子和原子均可再分
该化学反应中,甲、丁两种分子的个数比是
(3)胃酸过多须服用抗酸药。下表为两种抗酸药的有效成分及其构成微粒:
| 抗胃酸药 |
复方氢氧化镁片剂 |
铝碳酸镁片 |
| 有效成分 |
||
| 构成微粒 |
由于抗酸药有效成分不同,起抗酸作用(即消耗胃液中盐酸)的微粒也有差异。
①
起抗酸作用的微粒是
②铝碳酸镁与盐酸的反应为:
↑。则铝碳酸镁起抗酸作用的两种微粒是
二氯异氰脲酸钠(
)是一种预防
禽流感的有效消毒剂。下图为某工厂生产的二氯异氰脲酸钠产品的标签。

(1)1%的二氯异氰脲酸钠溶液呈性(填"酸"或"碱")。
(2)25
时,饱和二氯异氰脲酸钠溶液的溶质质量分数为。
(3)已知:
相对分子质量为220。请计算分析,标签中"有效氯(
%)≥60%"是否为
中氯元素的质量分数。计算过程(列出计算式即可):。结论:"有效氯(
%)"(填"是"或"不是")指
中氯元素质量分数。
铁是生产、生活中应用广泛的金属材料。
(1)酸菜等酸性的食物不宜用铁质器具长期盛放,因为
(2)为减缓海水对铁质海轮外壳的腐蚀,制造海轮时,会在海轮船底四周镶嵌比铁更活泼的金属。下列金属适宜船底镶嵌的是
(3)对铁"发蓝"处理,其表面将形成致密氧化膜而有效避免腐蚀。
①致密氧化膜能有效阻止铁锈蚀的原因是
②"发蓝"过程的化学方程式如下,式中
的化学式为
③为检验"发蓝"处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质。由此可知该零件"发蓝"处理效果
据报道:我省某渔船在霞浦海域捕鱼时,船上4名进入船舱的船员突然中毒倒地。
医生介绍,船员中毒是因为吸入鱼虾高度腐烂产生的、高浓度的硫化氢(H2S)。已知,硫化氢是一种无色、剧毒、可燃性气体。
(1)鱼虾腐烂会产生硫化氢,与鱼虾富含
A.糖类 B.维生素 C.蛋白质
(2)实验室常用湿润的硝酸铅试纸检验H2S。已知硝酸铅[Pb(NO3)2]与H2S发生复分解反应,该反应的化学方程式为
(3)有同学建议,将燃着的蜡烛带入船舱,观察舱内气体是否燃烧,可确定船舱内H2S浓度是否较高。这一做法非常危险,因为
(4)若有渔民向你请教,如何避免进入堆放鱼虾的密封船舱因吸入高浓度的H2S而中毒。你的一条建议是
下图装置用于制取某些气体。
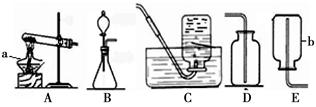
(1)填写下列仪器的名称:
a:
b:
(2)若用
制取氧气,反应的化学方程式为
(3)虽然常温常压下乙烯(
)不与空气反应,但因密度很接近空气而不用排空气法收集。若用排空气法收集乙烯,将
小李在化学实验技能考查中,完成"用稀盐酸鉴别氢氧化钠溶液和碳酸钠溶液,并测碳酸钠溶液的
"实验。
【实验一】小李取待测液甲、乙分别放置在试管①和②,再往两支试管中滴入稀盐酸,观察实验现象。根据现象推知,乙为碳酸钠溶液。

(1)实验中,小李应观察到试管②的现象是
该试管中反应的化学方程式为
(2)老师指出:除盐酸外,还可使用其它试剂鉴别氢氧化钠和碳酸钠溶液。请你选择一种不属于酸的试剂,并将鉴别实验中的预期现象以及化学方程式填入下表。
| 选择的试剂 |
预期现象 |
反应的化学方程式 |
|
|
一支试管无明显现象; 另一支试管 |
|
【实验二】小李用玻璃棒蘸取"实验一"后试管②中的溶液沾在
试纸上,观察试纸颜色变化并与标准比色卡对照,读出溶液的
。小李的记录如下:
| 实验现象 |
结论 |
| 溶液沾在试纸上时,试纸缓慢地变色 |
与标准比色卡对比,
溶液
|
(3)小李因操作错误,得出"
溶液
"的错误结论。指出小李操作错误之处。
答:
(4)指出小李记录的"实验现象"中不科学的地方。
答:

 粤公网安备 44130202000953号
粤公网安备 44130202000953号