内蒙古赤峰市元宝山区高二上学期期末化学试卷
2011年7月21日,世界各国领导人在南非德班共同商讨应对气候变化的道路——“拯救人类的最后机会”。要想节能减排下列属最有希望的新能源是( )
①天然气;②煤;③石油;④水能;⑤太阳能;⑥地热能;⑦风能;⑧氢能
| A.①②③④ | B.⑤⑥⑦⑧ | C.③④⑤⑥ | D.除①②外 |
下列说法不正确的是( )
| A.化学反应过程中,一定有化学键的断裂和形成 |
| B.盖斯定律实质上是能量守恒定律的体现 |
| C.反应前后原子种类和数目不变遵循的是质量守恒定律 |
| D.如果某化学反应的DH和DS均小于0,则反应一定能自发进行 |
在2A﹢B 2C﹢D反应中,表示该反应速率最快的是( )
2C﹢D反应中,表示该反应速率最快的是( )
A.v(A)=0.8mol·L-1·s-1 B.v(B)=0.3mol·L-1·s-1
C.v(C) =0.6mol·L-1·s-1 D.v(D)=0.5mol·L-1·s-1
下列各组物质的燃烧热相等的是( )
| A.碳和一氧化碳 |
| B.1 g碳和2 mol碳 |
| C.淀粉和纤维素 |
| D.3 mol乙炔(C2H2)和1 mol苯(C6H6) |
下列变化属于吸热反应的是 ( )
①液态水汽化
②将胆矾加热变为白色粉末
③浓硫酸稀释
④氯酸钾分解制氧气
⑤生石灰跟水反应生成熟石灰
⑥Ba(OH)2·8H2O与NH4Cl晶体混合
| A.①④⑤ | B.①②④ | C.①②⑥ | D.②④⑥ |
已知热化学方程式:SO2(g)+  O2(g)
O2(g)  SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
| A.196.64kJ | B.196.64kJ/mol | C.<196.64kJ | D.>196.64kJ |
汽车的启动电源常用铅蓄电池,电池反应如下:
PbO2 + Pb + 2H2SO4  2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是( )
2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是( )
| A.PbO2放电时是电池的负极,充电时是电池的阳极。 |
B.负极的电极反应式为:Pb + SO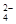 – 2e – = PbSO4 – 2e – = PbSO4 |
| C.放电时,PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |
在一密闭容器中,反应 aA(g) bB(g)+cC(g) 达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的40%,则( )
bB(g)+cC(g) 达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的40%,则( )
| A.平衡向正反应方向移动了 | B.平衡向逆反应方向移动了 |
| C.物质B的质量分数减小了 | D.a>b+c |
如下图各烧杯中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )
| A.④>②>①>③ | B.②>①>③>④ | C.④>②>③>① | D.③>②>④>① |
图中,用石墨作电极电解饱和氯化钠溶液,Cl2被完全吸收制得有效成分为NaClO的消毒液。下列说法正确的是( )
| A.a为正极,b为负极 | B.a为负极,b为正极 |
| C.a为阳极,b为阴极 | D.a为阴极,b为阳极 |
在蒸发皿中加热蒸干再加热(低于400℃)下列物质的溶液,可以得到该物质固体的是( )
| A.氯化铝 | B.碳酸氢钠 | C.硫酸亚铁 | D.硫酸镁 |
对可逆反应4NH3(g)+ 5O2(g) 4NO(g)+ 6H2O(g),下列叙述正确的是( )
4NO(g)+ 6H2O(g),下列叙述正确的是( )
| A.达到化学平衡时,4υ正(O2)= 5υ逆(NO) |
| B.若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态 |
| C.达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大 |
| D.化学反应速率关系是:2υ正(NH3)= 3υ正(H2O) |
已知下列热化学方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=-24.8kJ·mol-1
②Fe2O3(s)+ CO(g)=
CO(g)= Fe3O4(s)+
Fe3O4(s)+ CO2(g)ΔH=-15.73kJ·mol-1
CO2(g)ΔH=-15.73kJ·mol-1
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH=+640.4kJ·mol-1
则14 g CO气体还原足量FeO固体得到Fe固体和CO2气体时对应的ΔH约为( )
| A.-218kJ·mol-1 | B.-109kJ·mol-1 |
| C.+218kJ·mol-1 | D.+109kJ·mol-1 |
反应N2O4(g)  2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强的变化曲线如图所示。下列说法正确的是 ( )
2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强的变化曲线如图所示。下列说法正确的是 ( )
| A.a、c两点的反应速率:a>c |
| B.a、c两点气体的颜色:a深,c浅 |
| C.b、c两点的平衡常数:b<c |
| D.a、c两点气体的平均相对分子质量:a>c |
已知常温下BaSO4的溶解度为2.33×10-4g,类似于水的离子积,难溶盐AmBn也有离子积Ksp且Ksp=〔C(An+)〕m·〔C(Bm-)〕n,,则BaSO4的Ksp约为
| A.2.33×10-4 | B.1×10-5 | C.1×10-10 | D.1×10-12 |
在一密闭容器中,用等物质的量的A和B发生如下反应:A(g)+2B(g)  2C(g),反应达到平衡时,若混合气体A和B的物质的量之和与C的物质的量相等,则这时A的转化率为 ( )
2C(g),反应达到平衡时,若混合气体A和B的物质的量之和与C的物质的量相等,则这时A的转化率为 ( )
| A.40% | B.50% | C.60% | D.70% |
将0.2 mol/L NaA溶液和0.1 mol/L盐酸等体积混合后,溶液pH>7,以下关系式错误的是A.c(A-)> c(HA) B.c(Na+)+c(H+)= c(A-)+c(Cl-)+c(OH-)
C.c(HA)+c(A-)=0.1mol/L D.c(Na+)= c(A-)+ c(HA)
α1和α2分别为A在甲、乙两个恒容容器中平衡体系A(g) 2B(g)和2A(g)
2B(g)和2A(g) C(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是( )
C(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是( )
| A.α1、α2均减小 | B.α1、α2均增大 |
| C.α1减小,α2增大 | D.α1增大,α2减小 |
室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法错误的是( )
| A.溶液中导电粒子的数目增加 |
B.溶液中 不变 不变 |
| C.醋酸的电离程度增大,但电离平衡常数Ka不变 |
| D.再加入10 mL pH=11的NaOH溶液,恰好完全中和 |
有①Na2CO3溶液 ②CH3COONa溶液 ③NaOH溶液各25mL,物质的量浓度均为0.1 mol/L,下列说法正确的是( )
| A.3种溶液pH的大小顺序是③>②>① |
| B.若将3种溶液稀释相同倍数,pH变化最大的是② |
| C.若分别加入25mL0.lmol/L盐酸后,pH最大的是① |
| D.若用Pt电极电解3种溶液一段时间后,pH均不变 |
反应A+B→C(△H<0)分两步进行:①A+B→X(△H>0),②X→C(△H<0)。下列示意图中,能正确表示总反应过程中能量变化的是( )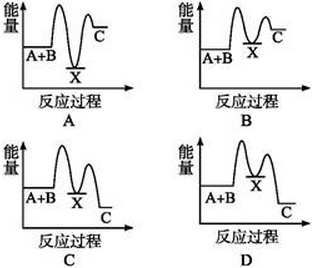
下列有关中和热的说法正确的是( )
| A.表示中和热的热化学方程式:H+(l)+OH-(l)=H2O(l) ΔH=-57.3 kJ/mol |
| B.准确测量中和热的实验过程中,至少需测定温度4次 |
| C.中和热的实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小 |
| D.已知2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ/mol,则该反应的中和热为114.6 kJ/mol |
向容积相同的甲、乙密闭容器中投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g) + 3H2(g)  2NH3(g) ΔH=-92.4 kJ·mol
2NH3(g) ΔH=-92.4 kJ·mol ):
):
| |
反应物投入量 |
NH3的浓度 (mol·L  ) ) |
反应的 能量变化 |
体系压强 (Pa) |
反应物 转化率 |
| 甲 |
1mol N2、3mol H2 |
c1 |
放出a kJ |
p1 |
α1 |
| 乙 |
2mol NH3 |
c2 |
吸收b kJ |
p2 |
α2 |
下列说法正确的是( )
A.c1 = c2 B.a + b =" 1" C.p1>p2 D.α1 +α2>1
已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1 kJ,又知胆矾分解的热化学方程式为:CuSO4·5H2O(s)  CuSO4(s)+5H2O(l) ΔH=+Q2 mol·L
CuSO4(s)+5H2O(l) ΔH=+Q2 mol·L 则Q1和Q2的关系为( )
则Q1和Q2的关系为( )
| A.Q1<Q2 | B.Q1>Q2 | C.Q1=Q2 | D.无法确定 |
以下是一些烷烃的燃烧热(kJ/mol)数据,回答下列问题:
| 化合物 |
燃烧热 |
化合物 |
燃烧热 |
| 甲烷 |
891.0 |
正丁烷 |
2 878.0 |
| 乙烷 |
1560.8 |
异丁烷 |
2 869.6 |
| 丙烷 |
2 221.5 |
2-甲基丁烷 |
3 531.3 |
(1)已知:物质的能量越高越不稳定,根据表中的数据,比较正丁烷、异丁烷的热稳定性:正丁烷______异丁烷(填“>”、“=”或“<”)。
(2)写出乙烷燃烧的热化学方程式:________________________
(3)相同质量的烷烃,碳的质量分数越大,燃烧放出的热量______(填“越多”、“越少”或“相同”)。
今有浓度均为0.1mol/L的醋酸、盐酸和硫酸三种稀溶液,按下列题示回答问题(回答时用“>”、“<”或“=”连接a、b、c):
(1)设三种溶液的pH分别为a、b、c,则大小关系为 。
(2)若取等质量的锌分别跟这三种溶液反应,使锌恰好完全反应时,所消耗三种酸的体积分别为a、b、c,则其大小关系为 。
(3)取上述三种溶液各10mL,分别跟0.1mol/LNaOH溶液10mL混合,当反应结束后,三种混合液的pH分别为a、b、c ,则其大小关系为 。
有人曾建议用AG表示溶液的酸度(acidity grade),AG的定义为
AG=lg(c(H+)/c(OH-))。请回答下列问题:
(1)在25℃时,若溶液呈中性,则AG= 。
(2)在25℃时,若溶液的pH=12,则AG= 。
(3)在25℃时,溶液的pH与AG的换算公式为AG= (要化简)。
(4)在25℃时,将AG=-12的NaOH溶液aL与AG=12的H2SO4溶液bL混合(混合后的体积误差可以 忽略),若所得混合液的AG=10,则a∶b= 。
某化学实验小组从市场上买来一瓶某品牌食用白醋(主要是醋酸的水溶液),用实验室标准NaOH溶液对其进行滴定以测定它的准确浓度。下表是4种常见指示剂的变色范围:
| 指示剂 |
石蕊 |
甲基橙 |
甲基红 |
酚酞 |
| 变色范围(pH) |
5.0~8.0 |
3.1~4.4 |
4.4~6.2 |
8.2~10.0 |
(1)该实验应选用 作指示剂。
(2)如图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为 mL;反应达滴定终点时的现象为 。
(3)为减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为c mo1/L,三次实验结果记录如下:
| 实验次数 |
第一次 |
第二次 |
第三次 |
| 消耗NaOH溶液体积/mL |
26.02 |
25.35 |
25.30 |
从上表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是 。
A.实验结束时,俯视刻度线读取滴定终点时NaOH溶液的体积;
B.滴定前滴定管尖嘴有气泡,滴定结束尖嘴部分充满溶液;
C.盛装白醋溶液的滴定管用蒸馏水洗过,未用白醋溶液润洗;
D.锥形瓶预先用食用白醋润洗过;
E.滴加NaOH溶液时,未充分振荡,刚看到溶液变色,立刻停止滴定。
(4)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不用化简):C1= mol/L。
10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
| 温度(℃) |
10 |
20 |
30 |
加热煮沸后冷却到50℃ |
| pH |
8.3 |
8.4 |
8.5 |
8.8 |
甲同学认为,该溶液的pH值升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为 。
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度 (填“大于”或“小于”)NaHCO3。
丙同学认为甲、乙的判断都不充分。丙认为:___________________________
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则 (填“甲”或“乙”)判断正确。试剂X是 。
A、Ba(OH)2溶液 B、BaCl2溶液 C、NaOH溶液 D、澄清石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH等于8.3,则 (填“甲”或“乙”)判断正确。
(3)常温下,在测得PH都等于9的NaOH溶液和Na2CO3溶液中,由水电离的OH—浓度分别为amol /L和bmol /L,则a与b的比值= 。
已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| 温度/ ℃ |
700 |
800 |
830 |
1000 |
1200 |
| 平衡常数 |
1.7 |
1.1 |
1.0 |
0.6 |
0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K= , △H 0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,若反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。,则6s时 c(A)= mol·L-1, C的物质的量= mol;
若经一段时间后,反应达到平衡,则此时A的转化率= ,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率 ( 填“变大”或“变小”或“不变”);
(3)判断该反应达到平衡的依据为 (填正确选项前的字母):
A.压强不随时间改变
B.气体的密度不随时间改变
C.c(A)不随时间改变
D.单位时间里生成C和D的物质的量相等
(4)1200℃时反应C(g)+D(g) A(g)+B(g)的平衡常数的值为 。
A(g)+B(g)的平衡常数的值为 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号