江苏省南京市、淮安市高三第二次模拟考试化学试卷
化学与人类生产、生活、社会可持续发展密切相关。下列说法正确的是
| A.减少CO2的排放,可以减少酸雨的产生 |
| B.减少SO2的排放,可以从根本上消除雾霾 |
| C.“天宫一号”使用的碳纤维,是一种新型有机高分子材料 |
| D.用CO2合成聚碳酸酯可降解塑料,可以实现“碳”的循环利用 |
下列化学用语表示正确的是
A.N2分子的电子式: |
B.中子数为18的氯原子的原子符号: |
C.CH4分子的球棍模型: |
D.HOCH2COOH缩聚物的结构简式 |
常温下在下列给定条件的溶液中,一定能大量共存的离子组是
| A.能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- |
| B.加入铝粉生成H2的溶液:K+、Mg2+、SO42-、HCO3- |
| C.c(Fe3+)=0.1 mol·L-1的溶液:H+、Al3+、Cl-、SCN- |
D. =0.1 mol·L-1的溶液:Na+、K+、SiO32-、NO3- =0.1 mol·L-1的溶液:Na+、K+、SiO32-、NO3- |
下列有关物质性质的应用错误的是
| A.药皂中加入少量苯酚,可以起到杀菌消毒的作用 |
| B.明矾能水解生成Al(OH)3胶体,可用作净水剂 |
| C.为防止月饼等富脂食品氧化变质,常在包装袋中放入生石灰 |
| D.NaHCO3受热能分解产生CO2气体,在食品工业中可作为焙制糕点的膨松剂 |
设NA为阿伏加德罗常数的值,下列说法中正确的是
| A.常温常压下,22.4 L乙烯中含C-H键的数目为4NA |
| B.0.1 mol·L-1的NaHSO4溶液中含有阳离子的总数为0.2NA |
| C.7.8 g Na2S固体和7.8 g Na2O2固体中含有的阴离子数目均为0.1NA |
| D.标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
下列有关实验正确的是
| A.图1:稀释浓硫酸 |
| B.图2:实验室制备氨气 |
| C.图3:实验室制备乙酸乙酯 |
| D.图4:检验浓硫酸与蔗糖反应产生的二氧化硫 |
下列表示对应化学反应的离子方程式正确的是
| A.用氯化铁溶液腐蚀铜板:Cu+Fe3+=Cu2++Fe2+ |
| B.碘水中通入适量的SO2:I2+SO2+2H2O=2I-+SO42-+4H+ |
| C.硝酸银溶液中滴加过量氨水:Ag++NH3·H2O=AgOH↓+NH4+ |
| D.往KAl(SO4)2溶液中滴入Ba(OH)2溶液至沉淀的物质的量最大: |
Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
甲、乙、丙、X是中学化学中常见的4种物质,其转化关系符合下图。其中甲和X不可能是
A.甲为C、X为O2
B.甲为Fe、X为Cl2
C.甲为SO2、X为NH3·H2O
D.甲为AlCl3溶液、X为NaOH溶液
短周期元素X、Y、Z、W原子序数依次增大,X原子最外层电子数是其电子层数的3倍,Y与X可形成Y2X2和Y2X两种离子化合物,Z原子的核外电子数比Y原子多1,W与X同主族。下列说法正确的是
| A.单质的还原性:Y>Z |
| B.原子半径:Y<Z<W |
| C.气态氢化物的稳定性:X<W |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
利用如图所示装置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液吸收NO2。下列说法正确的是
| A.a为直流电源的负极 |
| B.阴极的电极反应式为:2HSO3-+2H++e-=S2O42-+2H2O |
| C.阳极的电极反应式为:SO2+2H2O-2e-=SO42-+4H+ |
| D.电解时,H+由阴极室通过阳离子交换膜到阳极室 |
下列说法正确的是
| A.一定温度下,反应2NaCl(s)=2Na(s)+Cl2(g)的△H<0,△S>0 |
| B.温度一定时,向水中滴加少量酸或碱形成稀溶液,水的离子积常数Kw不变 |
| C.常温下,将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| D.由于Ksp(BaSO4)<Ksp(BaCO3),因此不可能使BaSO4沉淀转化为BaCO3沉淀 |
尿黑酸是由酪氨酸在人体内非正常代谢而产生的一种物质。其转化过程如下:
下列说法错误的是
| A.酪氨酸既能与盐酸反应,又能与氢氧化钠反应 |
| B.1 mol尿黑酸与足量浓溴水反应,最多消耗3 mol Br2 |
| C.对羟基苯丙酮酸分子中在同一平面上的碳原子至少有7个 |
| D.1 mol尿黑酸与足量NaHCO3反应,最多消耗3 mol NaHCO3 |
下列实验操作正确且能达到预期目的的是
| 选项 |
实验目的 |
操作 |
| A |
比较水和乙醇中羟基氢的活泼性强弱 |
用金属钠分别与水和乙醇反应 |
| B |
证明CH2=CHCHO中含有碳碳双键 |
滴入KMnO4酸性溶液 |
| C |
比较盐酸与醋酸的酸性强弱 |
分别测定同温同浓度NaCl与CH3COONa溶液的pH |
| D |
除去苯中混有的苯酚 |
向混合液中加入过量浓溴水,充分反应后,过滤 |
T℃时,在V L恒容密闭容器中加入足量的TaS2(s)和1 mol I2(g),发生反应TaS2(s)+2I2(g) TaI4(g)+S2(g) △H>0。t min时生成0.1 mol TaI4。下列说法正确的是
TaI4(g)+S2(g) △H>0。t min时生成0.1 mol TaI4。下列说法正确的是
A.0~t min内,v(I2)= mol·L-1·min-1 mol·L-1·min-1 |
| B.若T℃时反应的平衡常数K=1,则平衡时I2的转化率为2/3 |
| C.如图制备TaS2晶体过程中循环使用的物质是S2(g) |
| D.图中T1端得到纯净TaS2晶体,则温度T1<T2 |
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示[已知Ksp(CaC2O4)=2.3×10-9]。下列说法正确的是
| A.曲线①代表的粒子是HC2O4- |
| B.0.1 mol·L-1 NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) |
| C.pH=5时,溶液中主要含碳物种浓度大小关系为:c(C2O42-)>c(H2C2O4)>c(HC2O4-) |
| D.一定温度下,往CaC2O4饱和溶液中加入少量CaCl2固体,c(C2O42-)将减小,c(Ca2+)不变 |
工业上利用软锰矿浆烟气脱硫吸收液制取电解锰,并利用阳极液制备高纯碳酸锰、回收硫酸铵的工艺流程如下(软锰矿的主要成分是MnO2,还含有硅、铁、铝的氧化物和少量重金属化合物等杂质):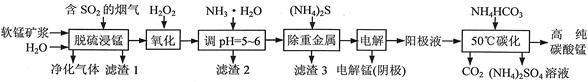
(1)一定温度下,“脱硫浸锰”主要产物为MnSO4,该反应的化学方程式为 。
(2)“滤渣2”中主要成分的化学式为 。
(3)“除重金属”时使用(NH4)2S而不使用Na2S的原因是 。
(4)“电解”时用惰性电极,阳极的电极反应式为 。
(5)“50℃碳化”得到高纯碳酸锰,反应的离子方程式为 。“50℃碳化”时加入过量NH4HCO3,可能的原因是:使MnSO4充分转化为MnCO3; ; 。
碘海醇是一种非离子型X-CT造影剂。下面是以化合物A(分子式为C8H10的苯的同系物)为原料合成碘海醇的合成路线[R-为-CH2CH(OH)CH2OH]:
(1)写出A的结构简式: 。
(2)反应①→⑤中,属于取代反应的是 (填序号)。
(3)写出C中含氧官能团的名称:硝基、 。
(4)写出同时满足下列条件的D的两种同分异构体的结构简式: 。
Ⅰ.含1个手性碳原子的α-氨基酸;
Ⅱ.苯环上有3个取代基,分子中有6种不同化学环境的氢;
Ⅲ.能发生银镜反应,水解产物之一能与FeCl3溶液发生显色反应。
(5)已知:
①
② 呈弱碱性,易被氧化
呈弱碱性,易被氧化
请写出以 和(CH3CO)2O为原料制备染料中间体
和(CH3CO)2O为原料制备染料中间体 的合成路线流程图(无机试剂任用)。
的合成路线流程图(无机试剂任用)。
合成路线流程图示例如下:H2C=CH2 CH3CH2Br
CH3CH2Br CH3CH2OH
CH3CH2OH
三氯异氰尿酸(结构简式如图)是一种极强的氧化剂和氯化剂。
(1)利用三氯异氰尿酸水解产物中的氧化性物质X可消毒灭菌,X的分子式为 。
(2)“有效氯”含量指从KI中氧化出相同量的I2所需Cl2的质量与指定化合物的质量之比,常以百分数表示。为测定三氯异氰尿酸的“有效氯”含量,现称取某三氯异氰尿酸样品0.5680 g,加水、足量KI、硫酸,配制成100 mL待测液;准确量取25.00 mL待测液于碘量瓶中,用0.1500 mol·L-1 Na2S2O3标准溶液滴定至溶液呈微黄色时,加入淀粉指示剂,继续滴定至终点(发生反应的方程式为:2Na2S2O3+I2=Na2S4O6+2NaI);重复测定2次,所得的相关数据如下表:
| 滴定序号 |
待测液体积/mL |
标准液滴定管起点读数/mL |
标准液滴定管终点读数/mL |
| 1 |
25.00 |
0.06 |
24.04 |
| 2 |
25.00 |
0.02 |
24.02 |
| 3 |
25.00 |
0.12 |
24.14 |
①滴定终点观察到的现象为 ;
②配制0.1500 mol·L-1 Na2S2O3溶液100 mL,所需Na2S2O3·5H2O的质量为 ;
③计算此样品的“有效氯”含量(写出计算过程)。
CoxFe3-xO4磁粉是一种比较好的高矫顽力磁粉。工业上以FeSO4为原料制备CoxFe3-xO4的主要步骤如下:
(1)步骤①是在FeSO4溶液中加入NaOH溶液,在40℃下搅拌生成FeOOH晶种。生成晶种的化学方程式为 ;
(2)步骤②将晶种移到放有FeSO4溶液和铁皮的生长槽中,升温到60℃,吹入空气,待晶种长大到一定尺寸后,过滤、水洗、干燥,得FeOOH粉末。生长槽中放入铁皮的目的是 ,吹入空气的作用为 。
(3)步骤③将FeOOH在200~300℃下加热脱水,生成红色Fe2O3。实验室完成该操作需要下列仪器中的 (填字母)。
a.蒸发皿 b.烧杯 c.坩埚 d.泥三角 e.酒精灯
(4)步骤④通入H2,加热至300~400℃,生成Fe3O4。通入H2前要向加热炉中通入N2,其作用为 。
(5)步骤⑤加入CoSO4溶液,所得粗产品经过滤、洗涤、干燥即得成品。检验粗产品洗涤干净的实验操作和现象是 。
(6)某研究小组欲用锂离子电池正极废料(含LiCoO2、铝箔、铁的氧化物)制备CoSO4·7H2O晶体。下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
| 金属离子 |
开始沉淀的pH |
沉淀完全的pH |
| Fe3+ |
1.1 |
3.2 |
| Fe2+ |
5.8 |
8.8 |
| Co2+ |
6.9 |
9.4 |
请完成下列实验步骤(可选用的试剂:H2O2、稀硝酸、稀硫酸、NaOH溶液):
①用N-甲基吡咯烷酮在120℃下浸洗正极废料,使LiCoO2与铝箔分离,得到LiCoO2粗品并回收铝。
② 。
③向所得粗品CoSO4溶液中加入NaOH溶液,调节pH约为5,过滤。
④ 。
⑤将Co(OH)2沉淀溶于稀硫酸中,蒸发浓缩、降温结晶,得到CoSO4·7H2O晶体。
LiBH4为近年来储氢材料领域的研究热点。
(1)反应2LiBH4=2LiH+2B+3H2↑,生成22.4 L H2(标准状况)时,转移电子的物质的量为 mol。
(2)下图是2LiBH4/MgH2体系放氢焓变示意图,则:
Mg(s)+2B(s)=MgB2(s) △H= 。
(3)采用球磨法制备Al与LiBH4的复合材料,并对Al-LiBH4体系与水反应产氢的特性进行下列研究:
①如图为25℃水浴时每克不同配比的Al-LiBH4复合材料与水反应产生H2体积随时间变化关系图。由图可知,下列说法正确的是 (填字母)。
a.25℃时,纯铝与水不反应
b.25℃时,纯LiBH4与水反应产生氢气
c.25℃时,Al-LiBH4复合材料中LiBH4含量越高,1000s内产生氢气的体积越大
②如图为25℃和75℃时,Al-LiBH4复合材料[ω(LiBH4)=25%]与水反应一定时间后产物的X-射线衍射图谱(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。
从图中分析,25℃时Al-LiBH4复合材料中与水完全反应的物质是 (填化学式),产生Al(OH)3的化学方程式为 。
(4)如图是直接硼氢化钠-过氧化氢燃料电池示意图。该电池工作时,正极附近溶液的pH (填“增大”、“减小”或“不变”),负极的电极反应式为 。
用Cr3+掺杂的氮化铝是理想的LED用荧光粉基质材料,氮化铝(其晶胞如图所示)可由氯化铝与氨经气相反应制得。
(1)Cr3+基态的核外电子排布式可表示为 。
(2)氮化铝的化学式为 。
(3)氯化铝易升华,其双聚物Al2Cl6结构如图所示。在Al2Cl6中存在的化学键有 (填字母)。
a.离子键 b.共价键 c.配位键 d.金属键
(4)一定条件下用Al2O3和CCl4反应制备AlCl3的反应为:Al2O3+3CCl4=2AlCl3+3COCl2。其中,COCl2分子的空间构型为 。一种与CCl4互为等电子体的离子的化学式为 。
(5)AlCl3在下述反应中作催化剂。分子③中碳原子的杂化类型为 。
对叔丁基苯酚 可用于生产油溶性酚醛树脂等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚的实验步骤如下:
可用于生产油溶性酚醛树脂等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚的实验步骤如下:
步骤1:按图16组装仪器,在X中加入2.2 mL叔丁基氯(过量)和1.41 g苯酚,搅拌使苯酚完全溶解。
步骤2:向X中加入无水AlCl3固体作催化剂,不断搅拌,有气体放出。
步骤3:反应缓和后,向X中加入8 mL水和1 mL浓盐酸,即有白色固体析出。
步骤4:抽滤得到白色固体,洗涤,用石油醚重结晶,得对叔丁基苯酚1.8 g。
(1)仪器X的名称为 。
(2)步骤2中发生主要反应的化学方程式为 。若该反应过于激烈,可采取的一种措施为 。
(3)图16中倒扣漏斗的作用是 。
(4)实验结束后,对产品进行光谱鉴定结果如下。其中属于红外光谱的谱图是 (填字母)。
(5)本实验中,对叔丁基苯酚的产率为 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号