高考化学苏教版总复习 专题10化学实验基础练习卷
在做化学实验时必须注意安全操作,下列实验操作或事故处理正确的是( )
①在点燃易燃气体前,必须检验气体的纯度 ②浓硫酸对皮肤有腐蚀性,如不慎溅到皮肤上,应用较多的水冲洗,再涂上硼酸稀溶液 ③给试管中的液体加热时,液体体积不超过试管容积的1/3 ④点燃添满酒精的酒精灯 ⑤用10 mL量筒量取8.55 mL蒸馏水
| A.仅① | B.仅①② | C.仅①③ | D.全部 |
在下列实验中,不能达到目的的是 ( )
| A.Fe与Cl2反应生成FeCl3,Fe与S反应生成FeS,确定非金属性:Cl>S |
| B.用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合溶液,确定铜和镁的金属活动性强弱 |
| C.进行H2O和H2S的热分解实验,确定硫和氧两种元素的非金属性强弱 |
| D.用pH试纸测定氯水的酸碱性 |
除去下列括号内杂质的试剂或方法错误的是 ( )
| A.HNO3溶液(H2SO4),适量BaCl2溶液,过滤 |
| B.CO2(SO2),酸性KMnO4溶液、浓硫酸,洗气 |
| C.KNO3晶体(NaCl),蒸馏水,结晶 |
| D.C2H5OH(CH3COOH),加足量CaO,蒸馏 |
下表中的实验,“操作和现象”与“结论”对应关系正确的一组是 ( )
| |
操作和现象 |
结论 |
| A |
向纯碱中滴加足量浓盐酸,将所得气体通入苯酚钠溶液中,溶液变浑浊 |
酸性:盐酸>碳酸>苯酚 |
| B |
取某溶液少量,加入经盐酸酸化的BaCl2溶液,出现白色沉淀 |
该溶液中一定含有大量的SO42— |
| C |
取少量Fe(NO3)2试样加水溶解后加稀H2SO4酸化,滴加KSCN溶液,溶液变为红色 |
该Fe(NO3)2试样已经变质 |
| D |
取皂化反应后的混合液滴入盛水的烧杯中,在液体表面出现油滴 |
皂化反应不完全 |
下述实验能达到预期目的的是 ( )
| |
实验内容 |
实验目的 |
| A |
向NaOH溶液中滴加FeCl3饱和溶液 |
制备Fe(OH)3胶体 |
| B |
向AgCl和水的混合物中滴加KI溶液,产生黄色沉淀 |
验证溶解度AgI小于AgCl |
| C |
淀粉溶液和稀硫酸混合加热后,加新制的Cu(OH)2悬浊液加热至沸腾 |
检验淀粉水解是否完全 |
| D |
将乙醇与浓硫酸共热,制得的气体通入酸性高锰酸钾溶液中 |
检验气体中有乙烯 |
下列化学实验事实及其解释都正确的是( )
| A.向KMnO4溶液中滴加盐酸,KMnO4溶液的氧化能力增强。说明盐酸具有氧化性 |
| B.向澄清的AlCl3稀溶液中加入NaOH浓溶液,振荡,溶液仍为澄清。说明该两种溶液混合是物理变化 |
| C.向FeCl3溶液中加入过量Cu粉,振荡、静置,溶液由黄色变为绿色。说明Fe3+具有氧化性 |
| D.向CaCl2溶液中通入CO2,不产生白色沉淀。说明CaCO3能溶于水 |
下列实验方案能达到目的的是 ( )
| A.除去Fe粉中混有的I2:加热使I2升华 |
| B.除去NaCl固体中混有的MgCl2:加入KOH溶液后过滤,滤液蒸发结晶 |
| C.除去碳酸钠中混有的碳酸氢钠:加入过量的氢氧化钠溶液,蒸发结晶 |
| D.除去氢氧化镁中混有的氢氧化钙:加入水中搅拌成浆状后,加入足量氯化镁溶液,加适量水过滤洗涤 |
下列实验方案不合理的是 ( )
| A.制硫酸和氢氧化钠:可用如图所示装置 |
| B.除去粗盐中的Ca2+、Mg2+、SO42—;依次加入的物质是H2O、Ba(OH)2、Na2CO3、HCl |
| C.检验Fe(NO3)2试样是否变质:取少量试样加水溶解,用稀硫酸酸化,滴加KSCN溶液 |
| D.乙醛的氧化:在试管里加入10%的NaOH溶液2 mL,滴入2%的CuSO4溶液4~6滴,振荡后加入乙醛溶液0.5 mL,加热至沸腾 |
为达到预期的实验目的,下列操作正确的是 ( )
①配制FeCl3溶液时,将FeCl3固体溶于盐酸中,然后再加蒸馏水稀释到所需的浓度 ②用10 mL量筒量取4.80 mL的浓硫酸 ③蒸发溶液时,边加热边搅拌,直至蒸发皿中的液体蒸干 ④向无色溶液中加BaCl2溶液,生成白色沉淀,再加稀硝酸,沉淀不消失,由此确定该溶液中一定含有SO42— ⑤为鉴别KCl、AlCl3和MgCl2溶液,分别向三种溶液中滴加NaOH溶液至过量 ⑥中和热测定的实验中使用的玻璃仪器只有2种 ⑦实验室可利用浓氨水和碱石灰混合的方法制取少量氨气 ⑧除NO中混有的NO2气体可通过水洗,再干燥后用向上排空气法收集 ( )
| A.③⑤⑧ | B.④⑤⑥ | C.①⑤⑦ | D.①⑦⑧ |
下列实验方案设计正确的是 ( )
| A.分解高锰酸钾制取氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤 |
| B.失去标签的AgNO3溶液、稀盐酸、NaOH溶液、AlCl3溶液可选用(NH4)2CO3溶液作鉴别试剂 |
| C.用铜丝代替铂丝做焰色反应 |
| D.在裂化汽油中加入酸性高锰酸钾,振荡后若紫色褪去即可证明其中含甲苯等苯的同系物 |
用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U形管的质量差,实验测得m(H):m(O)>1:8。下列对导致这一结果的原因的分析中,一定错误的是( )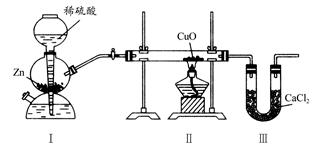
| A.Ⅰ、Ⅱ装置之间缺少干燥装置 |
| B.Ⅲ装置后缺少干燥装置 |
| C.Ⅱ装置中玻璃管内有水冷凝 |
| D.CuO没有全部被还原 |
下列有关实验的描述正确的是 ( )
| A.氢氧化钠固体保存在配有橡皮塞的细口瓶中 |
| B.将SO2通入品红溶液或KMnO4溶液均能使它们褪色,均可证明SO2有漂白性 |
| C.不能在石英坩埚中熔化氢氧化钠 |
| D.用湿润的pH试纸测定稀盐酸的pH |
关于下列各实验装置的叙述中,正确的是( )
| A.装置①制备乙酸乙酯 |
| B.装置②中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 |
| C.装置③可用于干燥、收集Cl2,并吸收多余的Cl2 |
| D.装置④配制一定物质的量浓度的溶液时转移液体 |
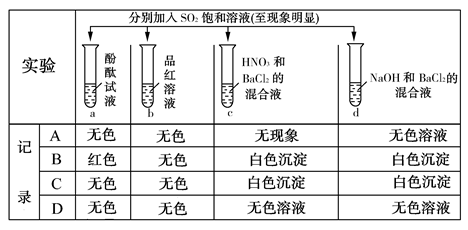
下列实验现象的解释正确的是 ( )
| |
实验现象 |
解释 |
| A |
KI淀粉溶液中通入Cl2,溶液变蓝 |
淀粉能与Cl2发生显色反应 |
| B |
浓硝酸在光照条件下变黄 |
浓硝酸见光分解,生成NO2溶于浓硝酸 |
| C |
某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 |
一定是由于该溶液中含有SO42— |
| D |
铜片放入冷的浓硫酸中,无明显变化 |
铜在冷的浓硫酸中发生钝化 |
下列各组溶液中,用括号内的试剂及物质间的相互反应不能鉴别的一组是( )
| A.Ba(OH)2 KSCN NaCl Mg(NO3)2 (FeCl3溶液) |
| B.NaNO3 NaHCO3 (NH4)2SO3 Na2SiO3 (H2SO4溶液) |
| C.NH4Br K2CO3 NaI CaCl2 (AgNO3溶液) |
| D.(NH4)3PO4 NaBr CuSO4 AlCl3 (KOH溶液) |
已知某酸性土壤浸取液中除Fe3+外,还含有一定量Mg2+和Al3+。请设计合理实验检验该浸取液中的Mg2+、Al3+。
限选实验用品与试剂;烧杯、试管、玻璃棒、滴管、玻璃片、pH试纸;浸取液、20%KSCN、0.1 mol·L-1 NaOH、6 mol·L-1 NaOH、0.1 mol·L-1 HCl、蒸馏水。
必要时可参考:
| 沉淀物 |
开始沉淀时的pH |
沉淀完全时的pH |
| Mg(OH)2 |
9.6 |
11.1 |
| Fe(OH)3 |
2.7 |
3.7 |
根据你设计的实验方案,叙述实验操作、预期现象和结论。(测定溶液pH的具体操作可不写)
| 实验操作 |
预期现象和结论 |
| 步骤1: |
|
| 步骤2: |
|
| 步骤3: |
|
| …… |
|
某化学兴趣小组的同学利用下图所示实验装置进行某些气体的制备、性质等实验(图中夹持装置有省略)。请按要求填空:

Ⅰ.探究氯气与氨气的反应
(1)为制取干燥氨气,可将装置C与________(填装置编号)连接;装置C中的烧瓶内固体宜选用________。
a.碱石灰 b.氯化钙 c.五氧化二磷 d.生石灰
(2)装置A、E、E连接可制取纯净、干燥的氯气,则两个E装置内的药品依次是________。
(3)装置F可用于探究氯气与氨气(已知氯气与氨气可发生反应:3Cl2+2NH3=N2+6HCl)的反应。实验时打开开关1、3,关闭2,先向烧瓶中通入________,然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的另一种气体。实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体中的阳离子________。
Ⅱ.探究某些物质的性质
(1)利用装置A、E,可设计实验比较Cl-和Br-的还原性强弱,能证明结论的实验现象是________。
(2)若利用装置A、E进行乙烯与溴水反应的实验,必须对装置A进行的改动是________。
(3)将装置B、C分别与F相连后,进行H2S与SO2反应的实验。F的烧瓶中发生反应的化学方程式为________________;F的烧杯所起的作用是_________。
某研究性学习小组在用CO还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X,他们认为X不一定是Fe,因为加热温度不同、受热不均时会生成Fe3O4,也能被磁铁吸引。为探究X的成分,他们进行了如下实验(图中①②表示试剂的加入顺序)。
(1)操作Z是________。下列仪器中,在灼烧沉淀时必须用到的仪器名称是________;
(2)写出向溶液Y中滴加H2O2溶液时发生反应的离子方程式:________;
(3)通过以上数据,得出2.376 g黑色粉末X中各成分的物质的量为________。
固态化合物A由两种短周期元素组成,可与水发生复分解反应,甲组同学用下图装置(夹持装置略)对其进行探究实验。
(1)仪器B的名称是________。
(2)实验中,Ⅱ中的试纸变蓝,Ⅳ中黑色粉末逐渐变为红色并有M生成,则Ⅲ中的试剂为________;Ⅳ中发生反应的化学方程式为________;V中的试剂为________。
(3)乙组同学进行同样实验,但装置连接顺序为ⅠⅢⅣⅡVⅥ,此时Ⅱ中现象为________,原因是________。
(4)经上述反应,2.5 g化合物A理论上可制得0.56 L(标准状况)M,则A的化学式为________。
化学兴趣小组设计以下实验方案,测定某已部分变质的小苏打样品中Na2CO3的质量分数。
方案一:称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为:________。
(2)实验中,需加热至恒重的目的是________。
方案二:称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3—=BaCO3↓+H2O)
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为________。
(2)实验中判断沉淀是否完全的方法是________。
方案三:按如下图所示装置进行实验:
(1)D装置的作用是________。分液漏斗中________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90 g样品,实验后测得C装置增重8.80 g,则样品中Na2CO3的质量分数为________。
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷,该缺陷是________。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号